星标“医工学人”,第一时间获取医工交叉领域新闻动态~


与许多阿尔茨海默症研究人员一样,神经学家兰德尔·贝特曼(Randall Bateman)在他的领域经历了失望。但他和其他人最近进行了一个让人感到兴奋的研究。他预测,在短短几年内,将有一个简单的血液测试来评估患阿尔茨海默症的风险。“任何家庭医生都能做到。”
8月7日,Nature期刊评论文章Blood tests could soon predict your risk of Alzheimer’s,介绍了科学家们寻找到的反映阿尔茨海默病进展的生物标志物。
贝特曼在密苏里州圣路易斯的华盛顿大学工作,从事与阿尔茨海默病相关的临床试验已有近20年。“根据我知道的情况来看,这是一个非常有可能的情况,”他说。“这就像去检查你的血液胆固醇,然后在水平太高时服用他汀类药物。
影响全球5500多万人的阿尔茨海默诊断和治疗的前景可能迎来的非同寻常的转变可以归结为两件事——这两件事在十年前都被许多人认为几乎是不可能的。首先,如果及早发现,可以减缓疾病的药物现在能够进入市场。其次,科学家们已经为阿尔茨海默氏症开发了相对便宜且高度准确的基于血液的生物标志物。
这些生物标志物——在血液或组织中发现的任何生物分子的统称,可以表明某人的医疗状态——不是治疗方法。它们正在彻底改变可能延缓甚至预防阿尔茨海默氏症的疗法的前景。它们会通过在症状和脑损伤开始之前抓住疾病来做到这一点。
这种充满希望的情景取决于能够治疗或延缓疾病的药物的进一步开发,如果及早发现的话。但即使是现在,生物标志物已经在进行改进临床试验,使研究人员能够在比以前更早的阶段测试干预措施。他们正在改变研究人员追踪疾病进程的方式,并更多地了解其基本病理学。“这些测试的开发速度是非同寻常的,”伦敦大学学院的神经学家乔纳森·肖特说。“大家感到非常兴奋。”
成功的标志
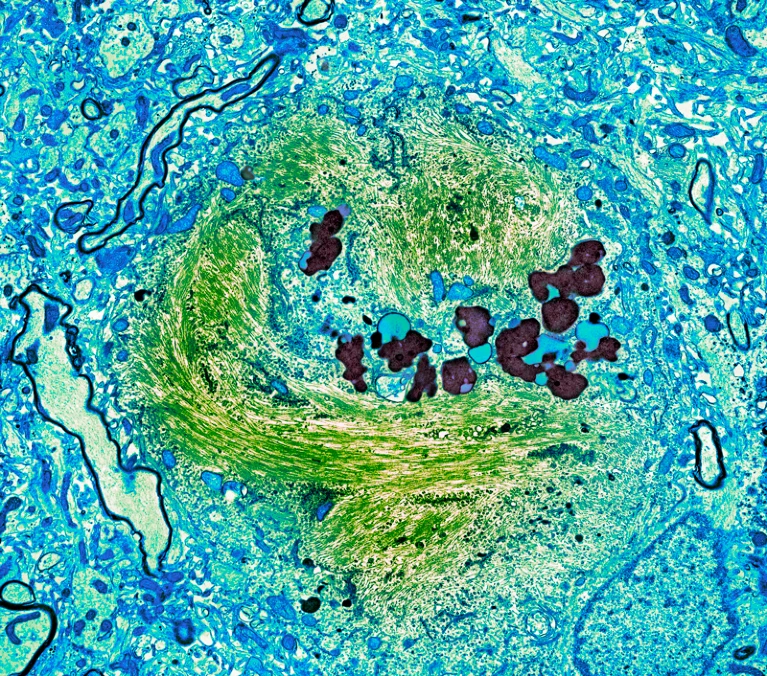
阿尔茨海默病患者神经元中的Tau蛋白缠结(绿色)。(来源:Nature)
阿尔茨海默病约占所有痴呆病例的三分之二。这类患者的大脑组织退化的地方有缝隙。该组织上点缀着斑块——被称为小胶质细胞的免疫细胞包围的粘性β淀粉样蛋白——并且上面缠绕着由 Tau 蛋白形成的细状缠结。
由于β淀粉样蛋白和Tau蛋白的生物标志物的发展,科学家们已经能够计算出病理的一般顺序。斑块首先形成,然后是Tau蛋白缠结,然后是症状。症状的严重程度与Tau蛋白缠结的程度相关。这个过程非常缓慢,以至于症状在斑块开始形成后 10 到 20 年才开始出现。
有缺陷的淀粉样蛋白可能是阿尔茨海默病的驱动因素的想法在 1990 年代获得了关注,当时科学家发现患有遗传性早发性疾病的家庭在参与淀粉样代谢的基因中发生了突变。数十项针对淀粉样蛋白的药物临床试验大张旗鼓地启动。当他们都失败时,一些科学家开始质疑淀粉样蛋白假说。
但药物本身可能不是问题所在。他们被交给了错误的人,或者为时已晚。在这些早期的试验中,研究人员没有很好的方法来选择参与者,选择适当的剂量或精确跟踪治疗效果。“那时,没有生物标志物,我们就是盲目的工作,”南加州大学圣地亚哥分校的神经学家保罗·艾森(Paul Aisen)说,他是美国阿尔茨海默氏症临床试验联盟的领导者。
阿尔茨海默病生物标志物可以在几个地方找到:在大脑中,在沐浴大脑和脊髓的脑脊液(CSF)中以及血液中。直到几年前,使用正电子发射断层扫描(PET)扫描大脑一直是金标准,与尸检时在显微镜下看到的病理密切相关。
当2004年淀粉样蛋白-PET脑部扫描问世时,“这产生了巨大的变化”,Aisen说。研究人员能够使用它来研究旨在抑制淀粉样蛋白的抗体 Aducanumab 的作用。“它首次表明,斑块确实是可以去除的。”
2016 年发表的 aducanumab 研究没有显示出明显的临床益处,而且该药物被证明会导致一些人出现微出血。但是,更安全的抗淀粉样蛋白抗体已经开发出来并在临床试验中进行了测试。一些试验表明,如果足够早地去除斑块,可以显著减缓疾病进展。
另一种类型的 PET 扫描是可视化 Tau,它是在 2010 年代中期被推出。有了这两种脑部扫描选项,两种类型的阿尔茨海默氏症病理(斑块和缠结)的数量和位置现在可以在活人身上看到,并随着时间的推移进行监测。
但是PET扫描非常昂贵且耗时,并且只能在专业医院进行。在抗淀粉样蛋白抗体在有脑斑块但没有症状的人中的首次临床试验中,A4试验,扫描 5,000 名候选人并选择最终参加的 1,169 人的成本约为 4000 万美元。
临床医生可以监测脑脊液中淀粉样蛋白的两个明显片段 Aβ40 和 Aβ42 以及各种 Tau 肽,而不是使用 PET 扫描来观察大脑本身。这些脑脊液标志物现在几乎与使用 PET 扫描一样准确,自 2022 年以来已被纳入美国食品和药物管理局的诊断指南。但监测脑脊液也有局限性,因为液体必须通过腰椎穿刺来获取,这是一个不舒服的过程,必须由专业人员进行。
为了避免这些并发症,科学家们长期以来一直在寻求开发针对与脑脊液检测相同的蛋白质生物标志物的血液检测。这种生物标志物将提供一种简单而廉价的方法,在脑损伤和症状开始之前识别患有阿尔茨海默氏症病理学的人。但是,开发这些测试非常具有挑战性,以至于“有时它似乎几乎像是一个神话般的目标”,Bateman说。
首先,生物标志蛋白在人体 5 升血液中的稀释度是人体 125 毫升脑脊液中的 40 倍。而且,与只清洗大脑和脊髓的脑脊液不同,血液中充满了来自身体各个部位的蛋白质。此外,尽管 Tau 蛋白的产生主要源头是大脑,但淀粉样蛋白是由许多器官中的细胞产生的,因此更难解释淀粉样蛋白的测量值。
自从淀粉样蛋白-PET扫描出现以来,数十篇声称在血液中发现了阿尔茨海默病信号的论文一直在文献中占据主导地位,但这些研究不一致且不可重复,瑞典隆德大学的神经学家Oskar Hansson说。“我们需要比脑脊液更灵敏的检测方法。”
这种检测方法分为两个阵营之一:一个使用粘附在淀粉样蛋白和Tau蛋白上的抗体;另一种依赖于质谱法,这是一种用于识别和量化复杂混合物中分子的方法。在过去十年左右的时间里,这两种方法的灵敏度都有所提高,以至于生物标志物检测现在可以始终如一地提供准确的结果。在 2010 年代中期,使用质谱法对两种淀粉样蛋白进行了首次准确可靠的血浆生物标志物检测。几年后,基于Tau的血浆生物标志物问世。
继续向下探索
研究人员继续寻找阿尔茨海默氏症蛋白的其他变体,这些变体可以提供更准确的生物标志物,特别是某些形式的Tau蛋白。
Tau的主要生物学功能之一是稳定神经元的内部,帮助形成称为微管的支架。随着阿尔茨海默病的进展,Tau蛋白变得越来越可溶并从微管中脱落。它们也会变得更粘,结块成原纤维。“这对神经元来说是毒性的双重打击,”英国爱丁堡大学的神经科学家Tara Spires-Jones说。
Tau分子化学性质的变化使其更易溶解:它变得布满磷酸基团,或被磷酸化。磷酸基团在蛋白质上的确切位置似乎具有生物学意义,并且在特定位置被磷酸化的Tau形式已被证明是有用的生物标志物。目前用于脑脊液诊断的 Tau 生物标志物 p-tau181 在 181 位被磷酸化。这种变体是第一个在血液中研究的Tau物种 ,但很快就找到了更好的选择。
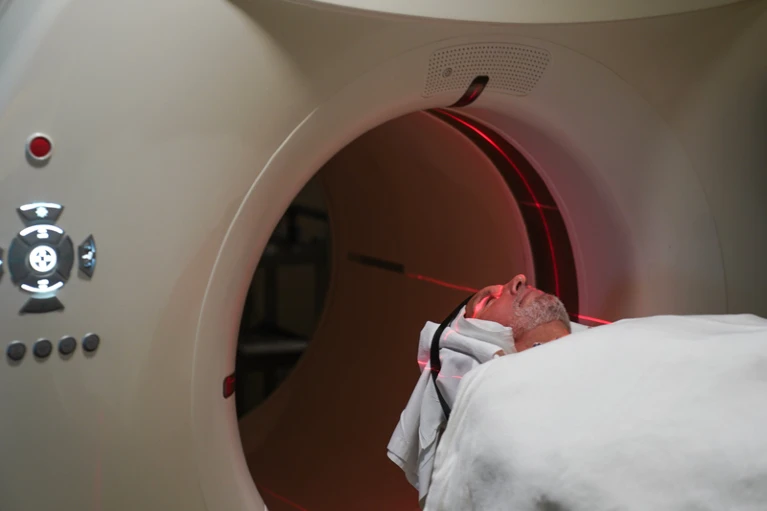
正电子发射断层扫描 (PET) 扫描可以观察大脑中的淀粉样斑块和 Tau 缠结,但它们价格昂贵且需要复杂的基础设施。(来源:Nature)
2019年初,Hansson决定分析来自瑞典BioFINDER-2队列的1,400多个储存血浆样本中的一种名为p-tau217的变体,该队列包括患有和没有痴呆症的人。那年11月,坐在一个会议上,他随便打开了一封来自他的一位博士后研究员的电子邮件。它载有研究的结果。“我惊呆了,”他回忆道。“p-tau217几乎100%肯定地预测了试验参与者的大脑中是否有阿尔茨海默病病理。他接下来要说话,但他的思绪混乱不堪,再也无法集中注意力。“这似乎好得令人难以置信。”
为了确保这确实是真实的,他和他的同事们一起分析了来自美国一个独立队列和哥伦比亚一个由遗传性早发性阿尔茨海默氏症患者组成的队列的样本。结果都排成一列,该研究发表了6在2020年7月。汉森记得有一段时间,工作紧张,没有假期。
此后,p-tau217的重要性已在许多其他临床研究中得到证实。事实上,它被证明是如此之好,以至于一些研究人员在没有伴随的淀粉样生物标志物的情况下在临床试验中使用它。但是,尽管这种蛋白质在诊断方面非常出色,但它已经引发了一个生物学之谜。
研究表明,它不仅与驱动疾病症状的 tau 缠结有关,还与淀粉样斑块负荷有关。科学家们曾认为,在阿尔茨海默症的进展中,淀粉样蛋白先于Tau蛋白,因此这一意想不到的观察结果使他们重新思考可溶性Tau蛋白在疾病中的作用。Hansson说,这表明淀粉样斑块直接诱导Tau被磷酸化的方式发生变化,并且Tau磷酸化的变化早在可见和破坏性的Tau缠结出现在大脑中之前就已经开始了。“这推动了旨在减少Tau产生疗法的发展,”他说。
但p-tau217并不是寻找生物标志物的终点。例如,它不能告诉临床医生太多关于某人的预后。“用于阿尔茨海默氏症诊断的p-tau217的开发使我们达到了PET的先前金标准,”Bateman说。“但是我们需要一系列的血液生物标志物 – 以帮助我们跟踪疾病的临床过程,并且当我们试图针对疾病的不同方面(如炎症)时,还可以告诉我们大脑中发生了什么。
科学家们对Tau分子中实际上将其锚定在缠结中的部分特别感兴趣。去年,贝特曼的团队为这个区域开发了一种测试,并表明它的存在与缠结和认知症状的严重程度有关。研究人员现在正在开发一种基于血液的检测方法。
扩大网络
其他液体生物标志物正在帮助追踪阿尔茨海默氏症病理学的更多方面,这可能有助于定义疾病分期或提供其他临床见解。“生物标志物在引导我们了解大脑在这种疾病中是如何变化方面非常有用的,”Spires-Jones说。
一种这样的生物标志物是一种蛋白质,它有助于维持神经胶质细胞的结构,神经胶质细胞本身为神经元提供支持。在病程中,胶质纤维酸性蛋白 (GFAP) 水平升高;当用抗体去除斑块时,它们会减少。测量GFAP可以预测所有类型痴呆症的未来认知能力下降。
另一种可以指示认知能力下降速度的蛋白质是神经丝轻链(NfL),它表明神经元正在分解。它的水平可以预测神经退行性变的强度,尽管像GFAP一样,它不能将阿尔茨海默氏症与其他类型的痴呆症区分开来。
研究人员越来越多地转向流行的“组学”技术,以推动对与阿尔茨海默症相关的更多分子的搜索。这些技术全面分析生物体中不同类型的分子,从基因到蛋白质。例如,二月份发表的一项蛋白质组学研究确定了至少三种与阿尔茨海默氏症新相关的蛋白质。“越来越多的信息丰富的血浆生物标志物使我们能够评估阿尔茨海默氏症在整个疾病谱中的神经生物学,”Aisen说。
加快试验速度
廉价和快速的血液生物标志物在阿尔茨海默症的临床试验中产生了很大的影响。他们已经在不失去准确性的情况下,使临床试验的招募变得更容易、更快捷。它们使临床医生能够选择那些受益最大的人,监测治疗对疾病的控制程度,并决定他们是否以及何时需要开始另一轮治疗。
在三种获批的阿尔茨海默氏症药物中,有两种的试验正在使用血液生物标志物来选择参与者并监测疾病。两种治疗方法都是抗淀粉样蛋白抗体:lecanemab 已在美国、日本和中国获得批准,donanemab 已在美国获得批准。在美国获得批准的早期药物aducanumab的试验进行得太早,无法利用血液标志物。
血液生物标志物将在这些药物和其他正在开发的淀粉样蛋白清除药物的新试验和正在进行的试验中发挥重要作用,使临床医生能够尽早招募到没有症状的人。如果不进行血液检查,就太困难且昂贵了。神经学家预测,在这个早期阶段对人们进行治疗,最有可能阻止疾病的蔓延。
甚至在这些药物被广泛使用之前,血液检测将成为临床医生的主要支持,临床医生仅根据症状分析,就会误诊大约四分之一的病例。在一项针对瑞典初级和二级保健中 1,200 多名认知障碍患者的研究中,获得血液检查结果的临床医生将他们的诊断准确性提高到90%以上。
Schott说,在英国,只有65%左右的痴呆症患者能够得到诊断,只有2%的人进行脑脊液测量或脑部扫描以进行分子诊断,因为记忆诊所没有能力进行这些测试。“然而,诊断对于计划、治疗选择甚至临床试验都非常重要。他正在领导一项对英国各地记忆诊所的1,100人进行的研究,以了解血液检测如何支持做出诊断的临床医生,以及这如何改善结果。该研究还将与伦敦政治经济学院合作,评估阿尔茨海默病早期诊断的成本效益。
十五年前,大多数制药公司缩减了他们的大脑研究,或者完全退出,看不到希望。但是,由于最近的突破,对阿尔茨海默病的行业投资又全面恢复了。“精灵现在已经从瓶子里出来了,”肖特说。“我们已经达到了一个临界点——阿尔茨海默病是一个可以被检测和治疗的生物过程。
▼扫码阅读英文原文

Nature 632, 243-245 (2024)
doi: https://doi.org/10.1038/d41586-024-02535-x
*文章仅为分享医工交叉领域前沿技术及动态,无任何利益关系。如涉及版权问题,请联系我们删除。
欢迎文末留言参与讨论~
END
编辑 | 罗虎
参考 | Nature
审核 | 医工学人理事会
扫码注册加入医工学人,进入综合及细分领域群聊,参与线上线下交流活动

*声明:医工学人为公益性非盈利组织,不收取任何注册费用
推荐阅读
穿戴未来:探索可穿戴超声设备的革命性应用 | 顶刊一文盘点(上)
点击关注医工学人


本篇文章来源于微信公众号: 医工学人