6 器官衰老与认知能力下降和AD
7 讨论
0 基本信息
-
标题:Organ aging signatures in the plasma proteome track health and disease -
期刊:Nature -
DOI:https://doi.org/10.1038/s41586-023-06802-1
1 摘要
-
动物研究表明,衰老在个体之间以及个体内部器官之间都有所不同,但这在人类身上是否属实及其对与年龄相关的疾病的影响尚不清楚。我们利用源自特定器官的人类血浆蛋白水平来测量活体个体的器官特异性衰老差异。 -
使用机器学习模型,我们分析了11个主要器官的衰老情况,并在包括5676名成年人的五个独立队列中可重复地估计了器官年龄。我们发现,近20%的人口在一个器官中表现出强烈的加速衰老,1.7%是多器官衰老者。器官衰老加速会导致20-50%的死亡风险,而器官特异性疾病与这些器官衰老加快有关。 -
我们发现,心脏老化加速的个体心力衰竭风险增加了250%,大脑和血管老化加速对阿尔茨海默病(AD)进展的预测独立于血浆pTau-181,并且与血浆pTau-181一样强烈,细胞外基质改变和突触蛋白脱落导致早期认知能力下降。我们介绍了一种简单且可解释的方法,利用血浆蛋白质组学数据研究器官衰老,预测疾病和衰老影响。
2 导读
-
衰老会导致整个生物体的组织结构和功能恶化,从而大大增加患大多数慢性疾病的风险。
-
对小鼠多个器官随衰老而发生的分子变化的全面研究已经确定了独特的分子衰老轨迹和时间,大脑、心脏和肾脏等特定器官对衰老疾病的易感性和恢复力在不同人群中差异很大。然而,人们对人体器官如何随着年龄的增长而发生分子变化知之甚少。对人体器官衰老的分子理解对于解决衰老带来的巨大全球疾病负担至关重要,并可能彻底改变患者护理、预防医学和药物开发。特别是,临床前研究表明,恢复活力的干预措施对器官的影响不同。为了将这些研究转化为变革性药物,我们必须能够准确地测量全身的衰老,并了解人类衰老的多样性,不仅在个体之间,而且在个体内部。 -
虽然已经开发了许多测量人类分子衰老的方法,但其中大多数方法只提供了一种测量全身衰老的单一方法。考虑到人类衰老轨迹的复杂性,这很难解释。最近的一些方法已经使用了包括一些器官功能标志物的临床化学标志物。 -
然而,这些标志物中的许多具有较低的器官特异性,使其难以解释器官特异性衰老。测量大脑老化的方法使用了基于MRI的大脑体积和功能连接测量成本较高,并且不能提供分子洞察力,或者具有所需的组织样本,这阻碍了它们在活体中的应用。在使用某些器官特异性血浆蛋白无创评估器官健康方面(如肝损伤的丙氨酸转氨酶)的丰富文献和临床实践的基础上,我们假设血浆中器官特异性蛋白的全面量化可以实现对任何器官的人体衰老的微创评估和跟踪。
3 血浆蛋白可以模拟器官衰老
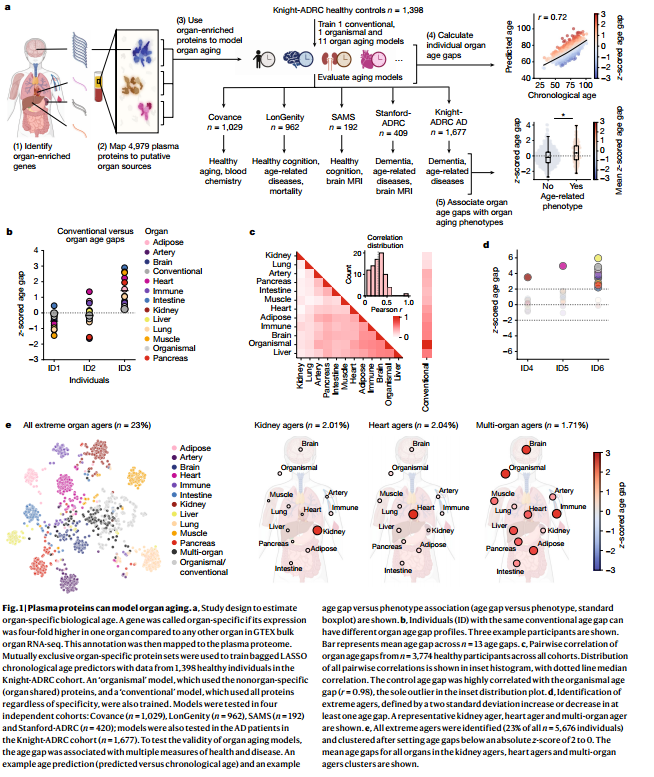
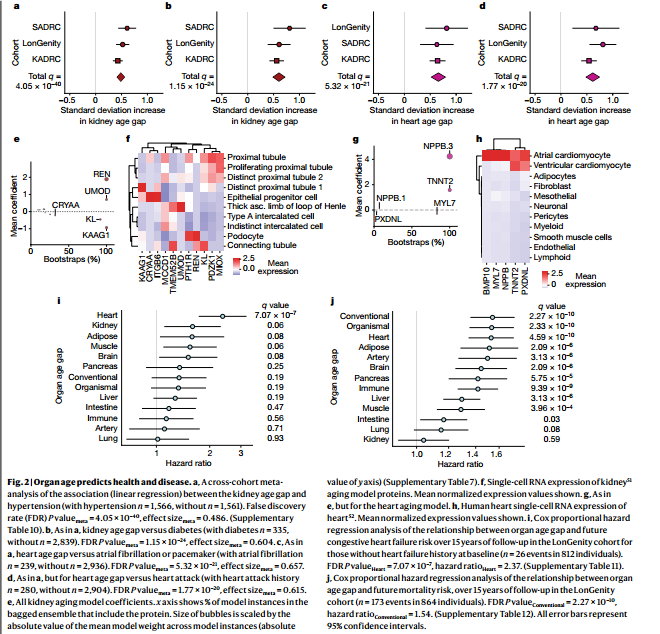
4 器官年龄预测健康和疾病
5 大脑衰老与认知能力下降和AD
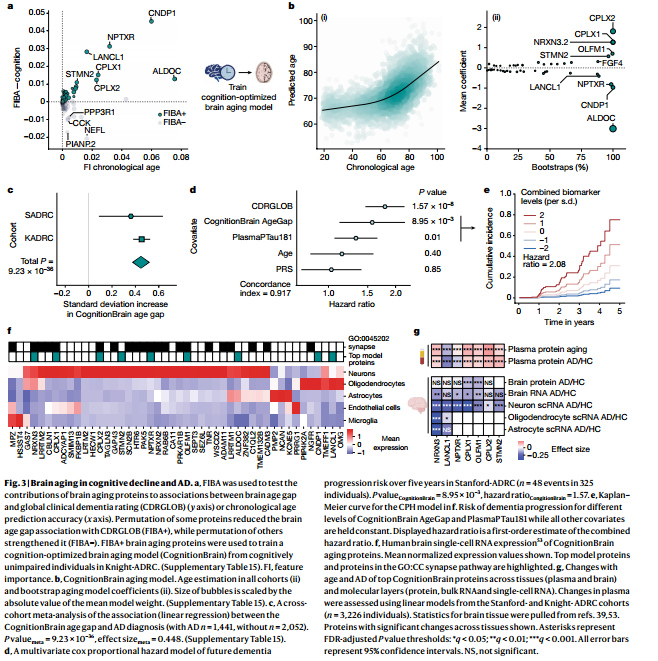
6 器官衰老与认知能力下降和AD
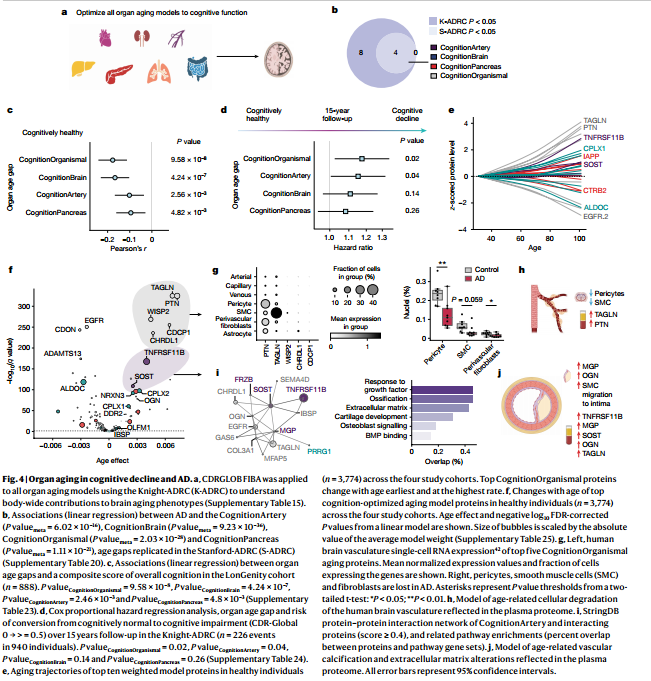
7 讨论
END
来源 | 第一作者EDesk
审核 | 医工学人理事会
推荐阅读
点击关注医工学人

本篇文章来源于微信公众号: 医工学人