前言
/
《医工前沿》是医工学人收集、整理与发布的医工交叉领域前沿研究动态,来源包括Science,Nature,The Lancet,IEEE,Advanced Materials等著名期刊及其子刊、合作刊等。医工交叉前沿动态的发布,有助于工程研究人员和临床医生迅速了解该领域学术前沿研究的最新现状,帮助医工领域研究者及从业者获得研究启发及转化可能。

研究背景

微型机器人凭借其体积小、质量轻、推重比大等特点,在循环系统中引导的微型机器人在精准医疗中提供了相当大的前景,但目前存在诸如对如何实现在血液高流速环境下高效驱动、如何实现循环系统内靶向释放等问题,降低了微型机器人在循环系统中对目标的富集和相互作用。
创新点
针对上述问题,哈尔滨工业大学机器人技术与系统全国重点实验室、哈尔滨医科大学第一附属医院等受到天然红细胞(RBC)的生物学特征和动态环境中水熊虫在软植物物质上的流动性的启发,设计并制备出具有爪几何形状、RBC膜伪装表面和磁力驱动保持的游泳微型机器人,以实现其在循环系统中更好的导航,最大限度地减少血流影响。爪接合设计无法为游泳微型机器人提供刚性基板上的最佳移动性,但它允许游泳微型机器人在流速< 2.1 cm/s的情况下的血管中的高效运动;xy平面中的磁驱动旋转允许游泳微型机器人在血液FR高达3.2 cm/s的血管中长时间停留,驻停时间大于36小时;此外,在游泳微型机器人上使用RBC膜涂层减少了与血流的相互作用,并有助于逃避免疫系统,从而使它们能够运动并保留在血管中。所有试验结论都为微型机器人在未来疗法中的应用创造了可观的前景。
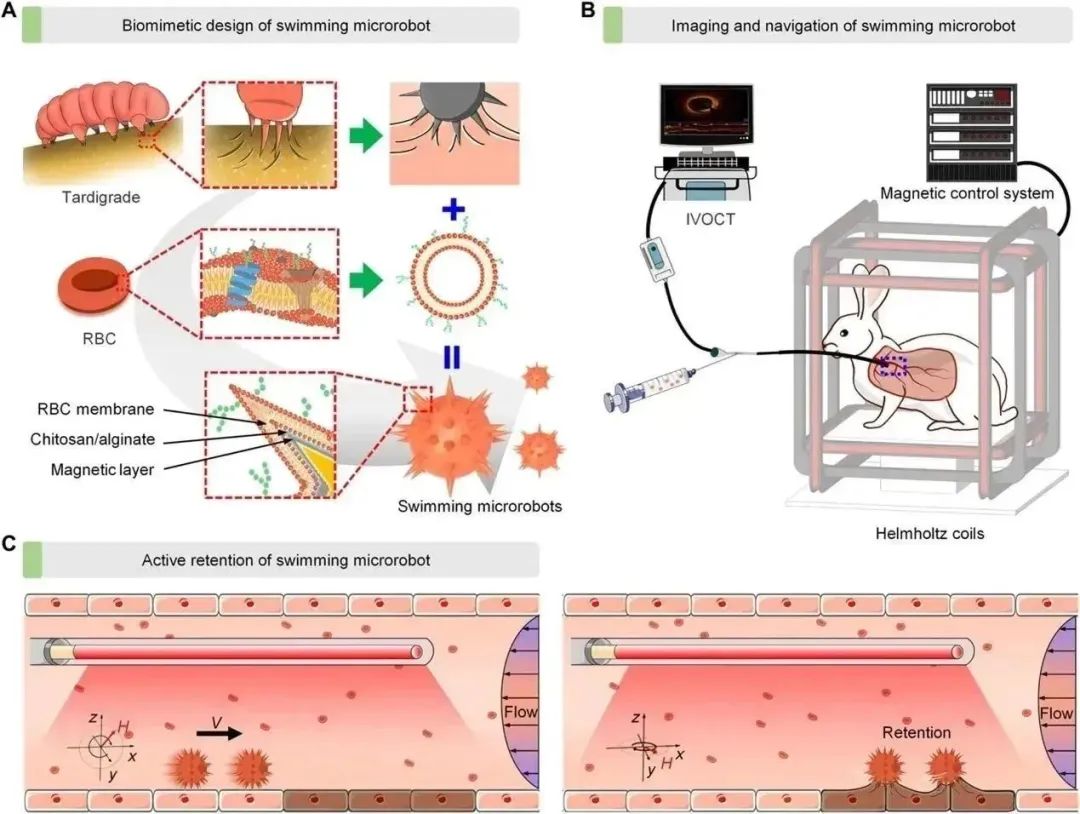
体内游泳微型机器人主动导航驻挺的示意图。(A)爪接合和生物润滑游泳微型机器人(CBSMRs)的概念开发。缓步动物启发了游泳微型机器人的爪形几何设计和磁致动爪啮合,红细胞(RBC)膜伪装涂层在游泳微型机器人上进行了功能化,以减少血流的影响。(B)兔体内血管中游泳微型机器人的成像和导航示意图。IVOCT,血管内光学相干断层扫描。(C)通过操纵外部磁场,在血管中导航运动和主动保留游泳微型机器人。
下面从三部分详细介绍该研究:
1. 游泳微型机器人的设计与制造
2. 磁致动游泳微型机器人在离体血管上的运动和驻停
3. 小鼠体内游泳微型机器人的磁动力学研究
4. 用IVOCT系统成像的游泳微型机器人在兔体内颈静脉上的主动导航保留
1
游泳微型机器人的设计与制造
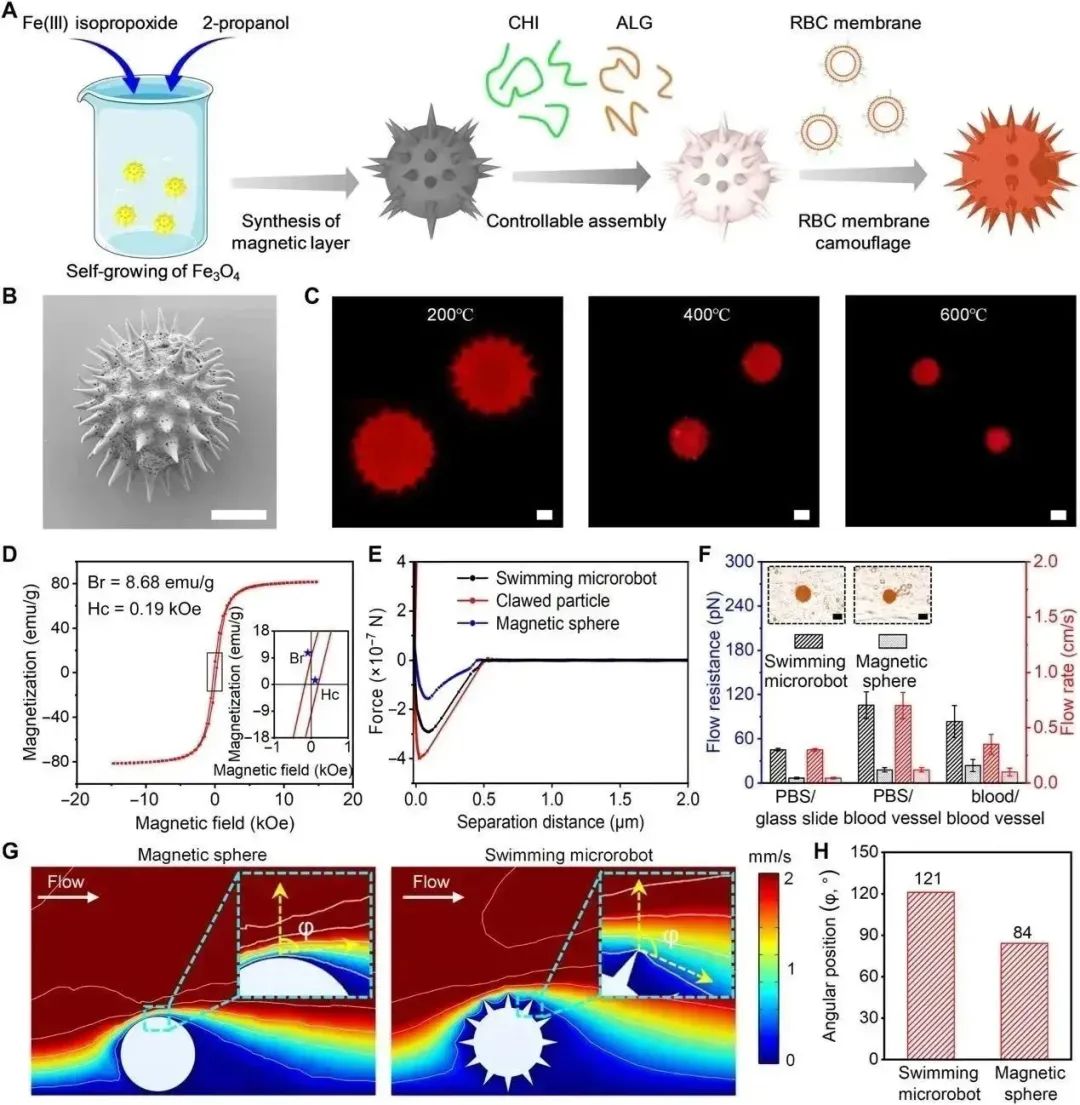
(A) 游泳微型机器人的制造步骤示意图,CHI,壳聚糖;ALG,藻酸盐;(B) 游泳微型机器人的扫描电子显微镜(SEM)图像,比例尺,10 μm;(C) 通过不同温度热处理获得的不同尺寸游泳微型机器人的荧光显微图像(RBC 膜用罗丹明 B染色),比例尺,5 μm;(D) 来自游泳微型机器人的超导量子干涉装置分析的磁化回路,Br,剩磁;Hc,矫顽力;emu,电磁单元;(E) 使用原子力显微镜(AFM)对游泳微型机器人的粘附力分析,磁性爪状颗粒(Clawed particle)和磁性球体(Magnetic sphere,MS)作为对照;(F) 游泳微型机器人可以提供的最大流动阻力,分别使用载玻片和血管作为基质,磷酸盐缓冲液(PBS)和血液作为流动介质(插图显示游泳微型机器人和相同尺寸的MS在血管表面的光学图像),比例尺,20 μm;(G) 游泳微型机器人和与其相同大小的MS在流动条件下的计算模拟流动剖面 [黄色箭头表示流动分离的角位置(φ 值)];(H) 游泳微型机器人和MS在水流中的角位置。
2
磁致动游泳微型机器人在离体血管上的运动和
驻停
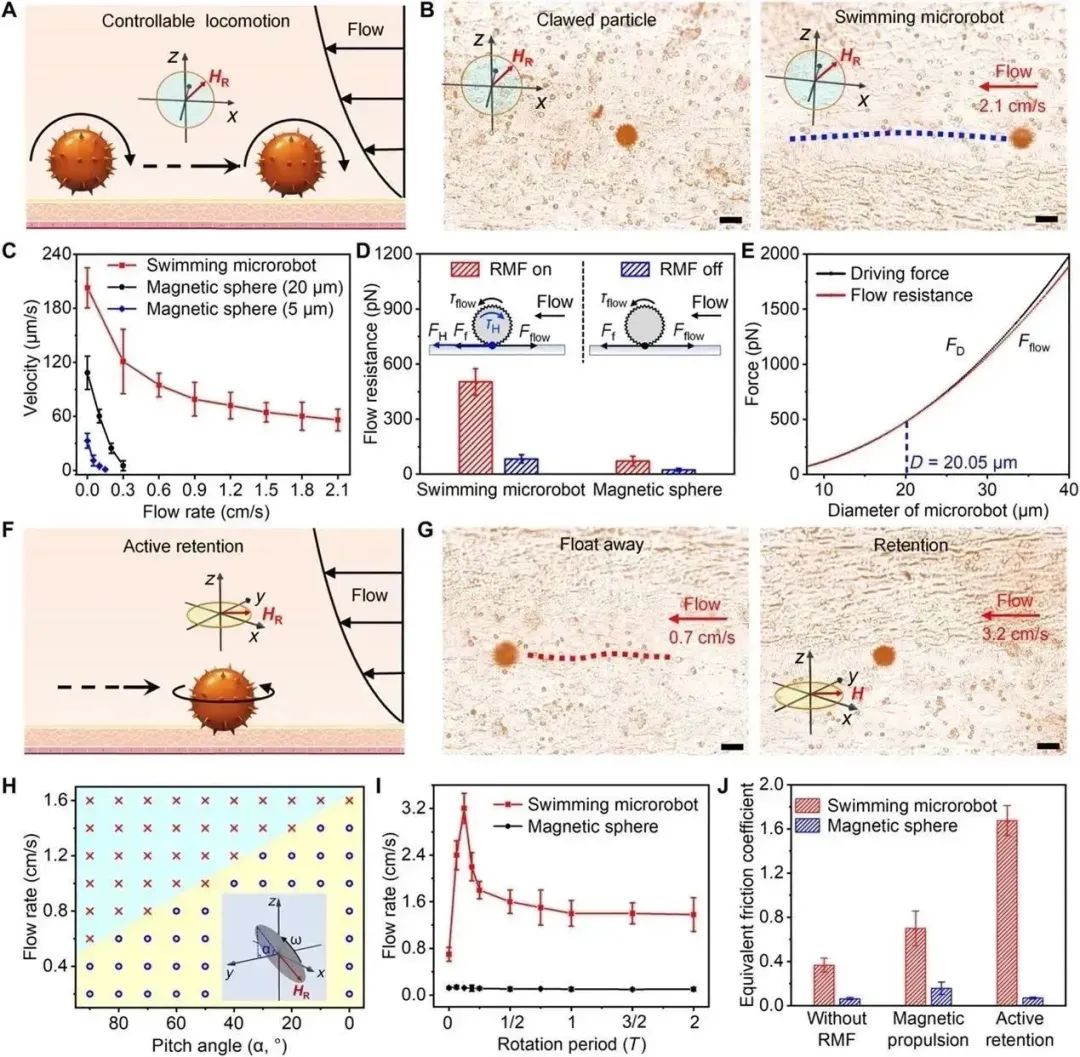
(A) 在xz平面的旋转磁场(RMF)下,微型游泳机器人在血管中的运动示意图;(B) 延时图像显示血管中磁性爪状颗粒(Clawed particle)和游动微型机器人的磁运动,流速(FR)为2.1 cm/s,蓝色虚线表示微型机器人向上游运动的路径,比例尺,30 μm;(C) 游泳微型机器人和MS(尺寸分别为 20 和 5 μm)的速度作为不同速率下流量的控制;(D) 具有最大FR的游泳微型机器人和MS的流动阻力,插图说明了RMF打开(左)和RMF关闭(右)的游泳微型机器人的力分析;(E) 磁驱动力和流动阻力对游泳微型机器人尺寸的依赖性(FR为2.1 cm/s);(F) 通过RMF的操作,磁力驱动的微型游泳机器人在血管中的滞留示意图;(G) 延时图像显示了在有血流的情况下游泳微型机器人和在xy平面上应用RMF的微型机器人的动力学,比例尺,30 μm,红色虚线表示微型机器人随血流飘走的运动路径;(H) 相图显示了在存在RMF的情况下,具有不同旋转角度的游泳微型机器人可以克服的FR;(I) 在流动存在、不同的旋转周期、旋转角度为0°的情况下,游泳微型机器人的驻停;(J) 具有不同磁驱动条件的游泳微型机器人的等效摩擦系数(EFC),MS作为对照。
3
小鼠体内游泳微型机器人的磁动力学研究
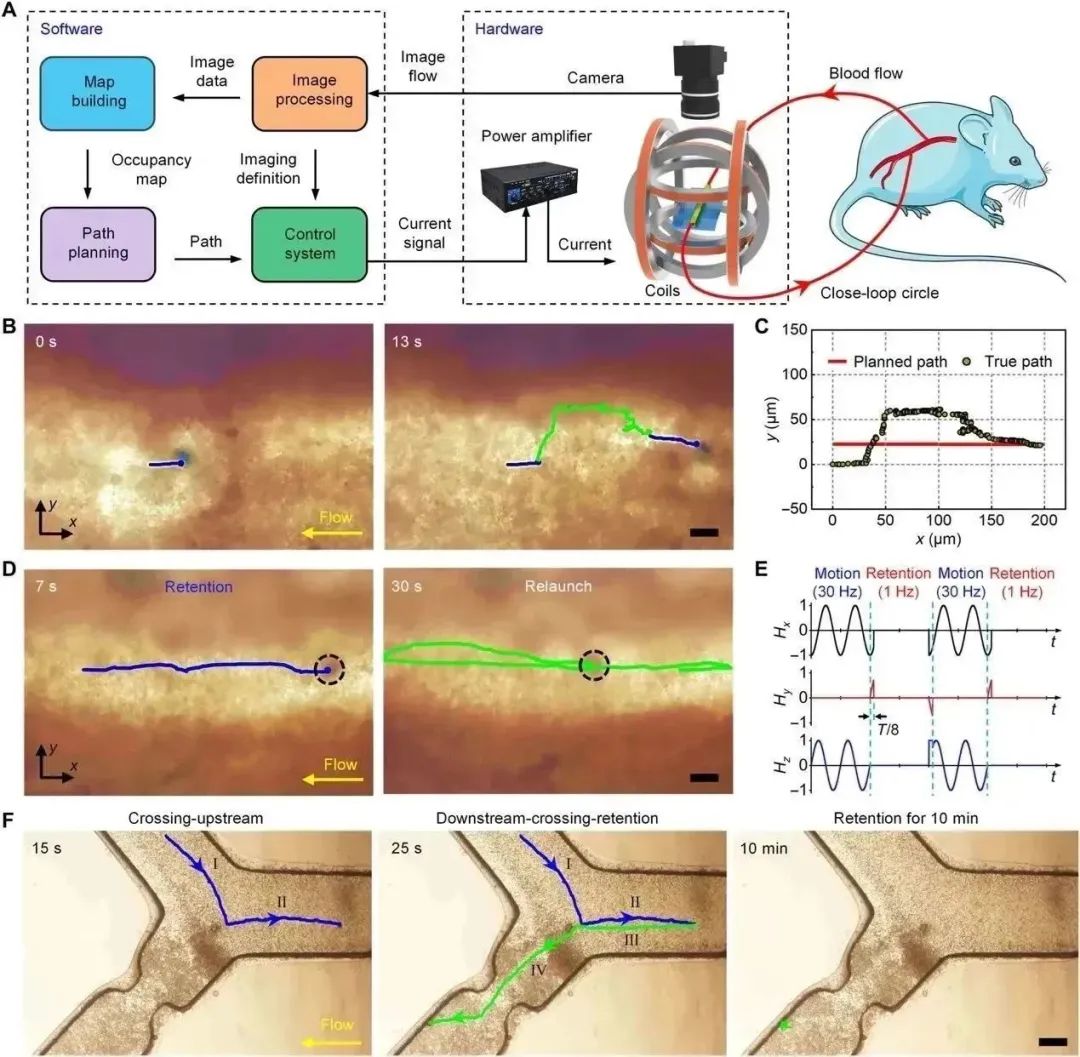
(A) 游泳微型机器人对小鼠血管的自主控制示意图;(B) 延时图像显示血管上游动微型机器人路径偏差的自我校正,蓝线和绿线分别代表微型机器人的正常磁驱动运动和路径自校正运动的轨迹,比例尺,50 μm;(C) 游泳微型机器人在路径自校正过程中的估计路径与自主导航实际路径的比较;(D) 显示游泳微型机器人在血管上的多次发射和滞留的延时图像,蓝线和绿线分别代表微型机器人在连续两次运动保持中的运动轨迹,比例尺,50 μm;(E) 两次运动保持对应的亥姆霍兹线圈x、y、z方向线圈组的输入电压信号;(F) 延时图像说明游泳微型机器人在与小鼠相连的模型血栓上的可控运动和延长保留,I-II-III-IV,穿越-上游-下游-穿越,比例尺,150 μm。
4
用IVOCT系统成像的游泳微型机器人在
兔体内颈静脉上的主动导航保留
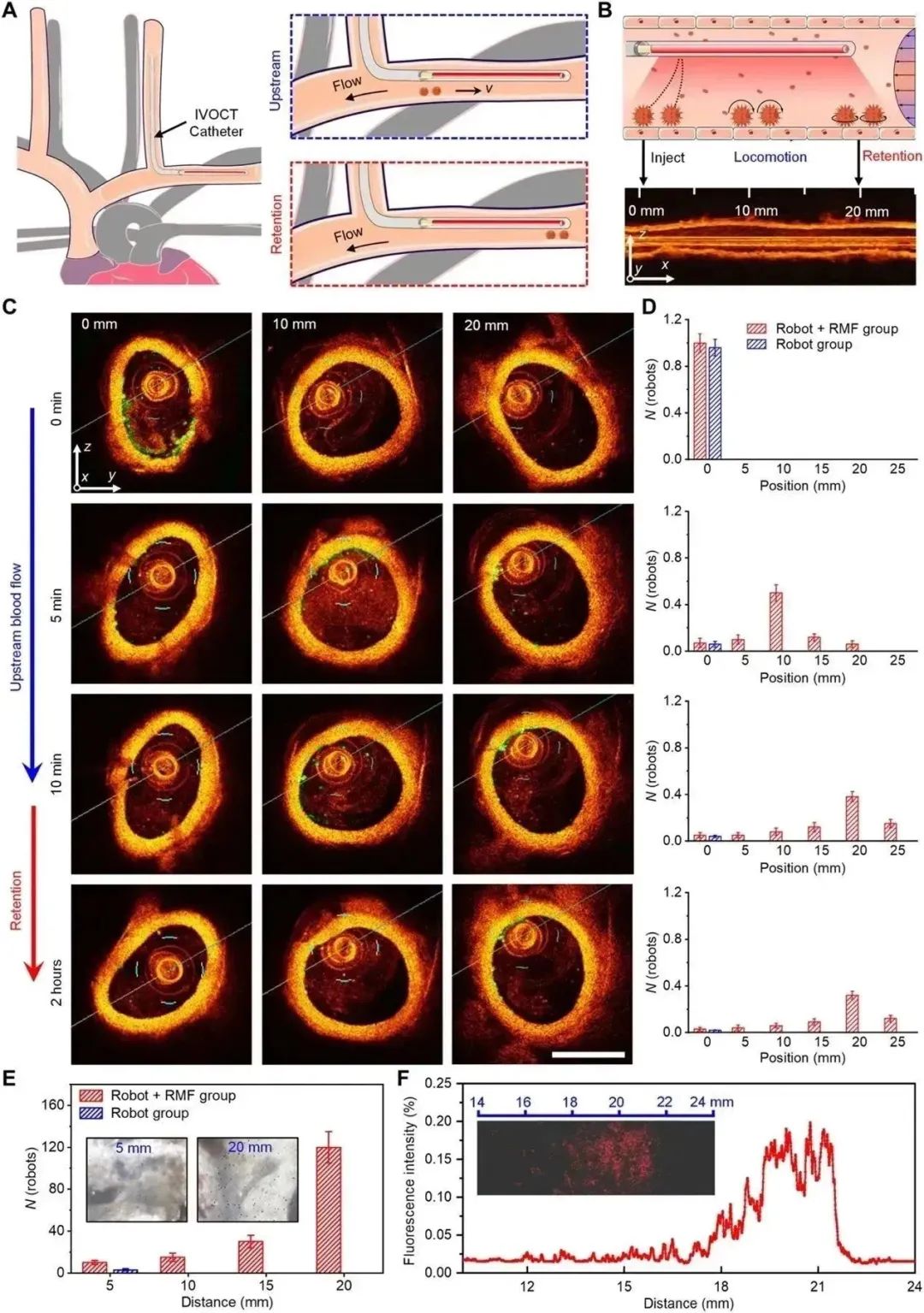
(A) 示意图说明了游泳微型机器人在血管上的定位和主动驻停的行为;(B) 体内游泳微型机器人的初始位置、运动和保持的示意图和 IVOCT 图像;(C) 游泳微型机器人(机器人+RMF组)在不同位置随时间变化的延时IVOCT图像,30 mT和30 Hz的RMF 在0~10 min内在yz平面上进行,在10 min时更改为xy平面,绿点表示来自游泳微型机器人的信号;(D) 从 (C) 中的绿点计算的游泳微型机器人的相应归一化数量,显示了在磁驱动运动和保持时游泳微型机器人在血管上的分布:实验统计数据是从对五只兔子进行的平行实验中总结出来的,误差条代表来自五次独立测量的SD,所有数据都归一化到它们的最大值,比例尺,1 mm;(E) 显微图像显示游泳微型机器人和控制MSs在体内血管上的主动驻停,比例尺,1 mm;(F) 体内主动导航驻停后游泳微型机器人分布的荧光分析。
研究意义
目前大部分研究使用治疗剂在循环系统中给药时,主要依赖于血流中的被动扩散。基于被动扩散的递送方法在体内密集血流下对靶标区域的粘附尤其具有挑战性。本文设计了一种设具有爪几何形状、RBC膜伪装表面和磁力驱动的游泳微型机器人,并通过实时血管内光学相干断层扫描(IVOCT)的微血管造影术和外部旋转磁场(RMF)的无线驱动,证实该游泳微型机器人不仅可以进行可控运动,也可在磁致动后在兔子的颈静脉中实现长期停留。该方案成功解决精准医疗发展进程中众多微纳材料在循环系统中的可控驻停、和高效富集等关键性问题,为化学疗法(药物递送)和物理疗法(光声、光热、光动力)的靶向控制提供新方案。
参考文章:
Tianlong Li et al., Bioinspired claw-engaged and biolubricated swimming microrobots creating active retention in blood vessels. Sci. Adv.9, eadg4501 (2023) . DOI:10.1126/ sciadv. adg 4501
https://www.science.org/doi/10.1126/sciadv.adg4501
▼扫描下方二维码阅读全文

END
作者 | 许静珂
编辑 | 徐嘉阳
审核 | 医工学人


本篇文章来源于微信公众号: 医工学人