*声明:本文仅分享医疗科技前沿最新动态,无任何利益关系。如涉及版权问题,请联系我们删除。
摘要
Abstrcats
肿瘤和癌前病变的早期发现对于癌症诊断至关重要。荧光显微技术和材料合成工艺的进步彻底改变了生物标志物检测和图像引导的癌症监测。特别是,基于新型材料的诊断工具和创新疗法促进了对分子水平上生物过程的精确理解。这篇批判性综述概述了生物成像探针,包括功能化发色团系统、非功能化发色团系统和纳米级生物传感器。并讨论了与这些方法相关的技术挑战和未来发展方向。
理论与方法
Theories and Methods
01
荧光生物成像的光物理机制
I. 聚集诱导发射
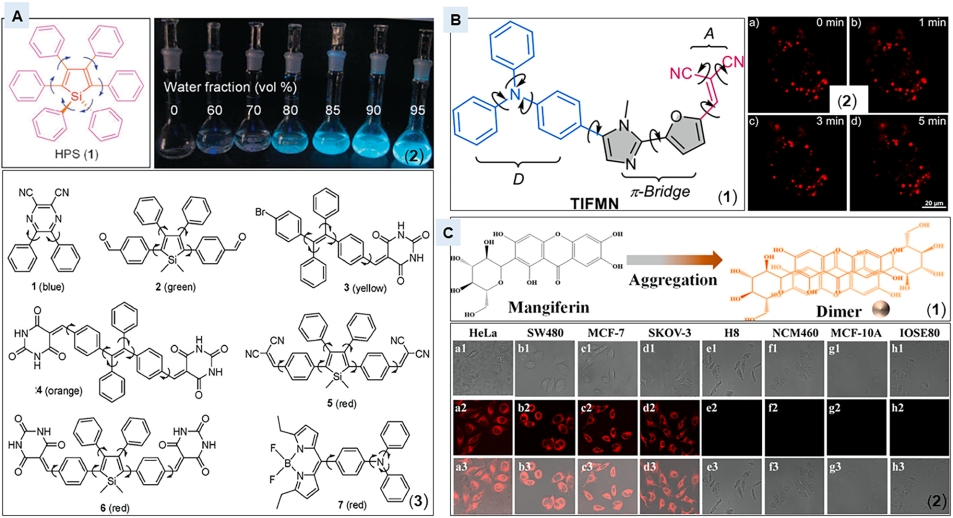
(A) AIE发光剂。
(B)AIE发光剂TIFMN的靶向组装,受体,供体与p桥偶联在一起
(C)(1)诱导芒果蛋白聚集(2)癌细胞及其相应正常细胞的共聚焦图像
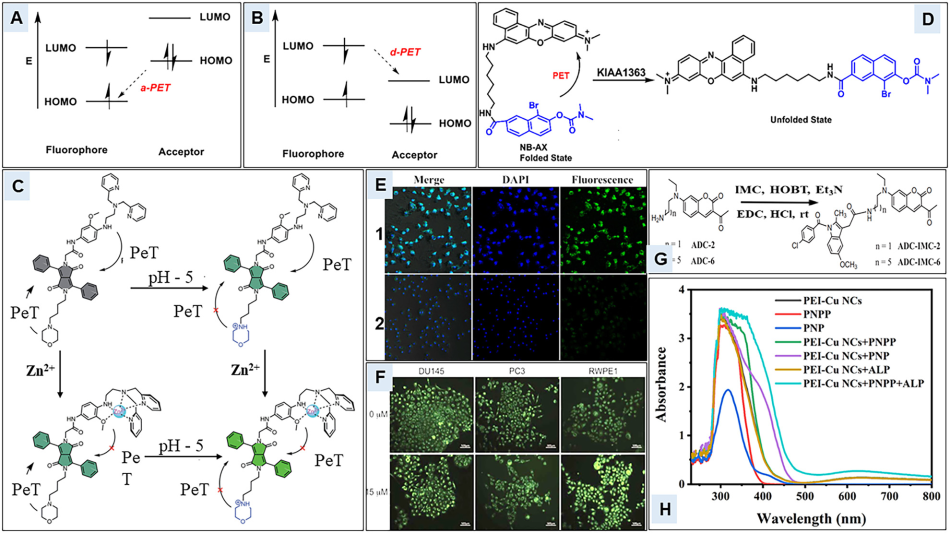
(A) 和 (B) PET 机理的能级图
(C)荧光“开启”机制示意图
(D) NB-AX的化学结构和传感机理
(E) 与 (1) PEI-Cu NCs 和 (2) PEI-Cu NCs + PNPP.106 一起孵育的 A549 细胞的共聚焦荧光图像
(F) 前列腺癌细胞 PC3 和 DU145 以及正常人前列腺上皮细胞 RWPE1 的荧光显微图像,
(G) ADC-IMC-2 和 ADC-IMC-6.109 的合成路线
(H)辅助试验的紫外-可见吸收光谱验证PNP的超致色效果
II. 光诱导电子转移
III. Forster共振能量转移
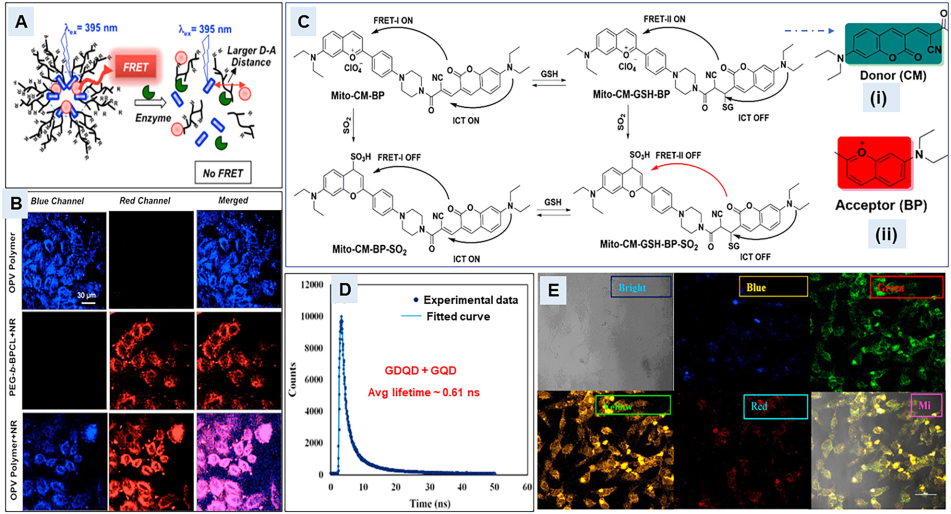
(A) 嵌段共聚物中PCL链段的酶促生物降解从FRET条件到无FRET条件的变化
(B) P30聚合物、NR 封装对照聚合物(聚合物 + NR)和 P30-NR 聚合物 (A)与 HeLa 细胞孵育的共聚焦图像
(C) GSH 和 SO2 传感的协同 FRET 和 ICT 过程,包括 (i) 供体,(ii) 受体中心.
(D) GDQD+GQD的荧光寿命衰减光谱
(E) MDA-MB 231 细胞在 405 nm 激发下与 GDQD-microRNA-21 一起孵育的荧光显微镜图像
IV. 上转换发光
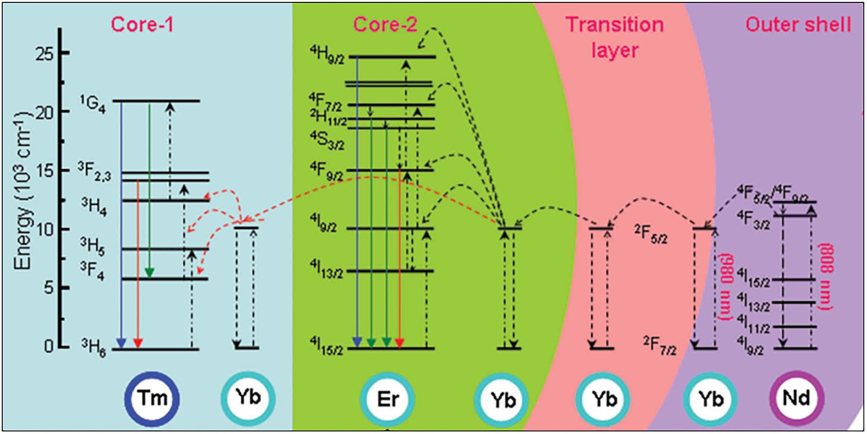
示意图显示了纳米哑铃中 980 和 808 nm 连续波 (CW) 激光激发下提出的能量传递机制.
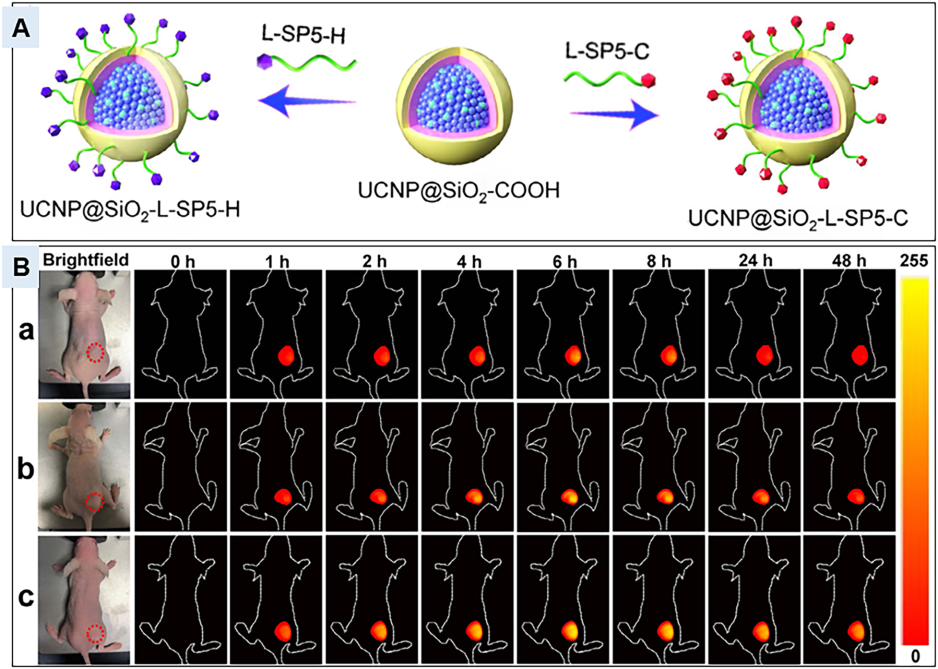
(A) 用于 UCL/MR 双模生物成像的肿瘤靶向肽修饰 UCNP 的示意图
(B) HCT116 荷瘤 BALB/c 裸鼠的体内 UCL 图像(a) UCNP@SiO2-COOH、(b) UCNP@SiO2-l-SP5-H 和 (c) UCNP@SiO2-l-SP5-C 分别在注射后的不同时间点
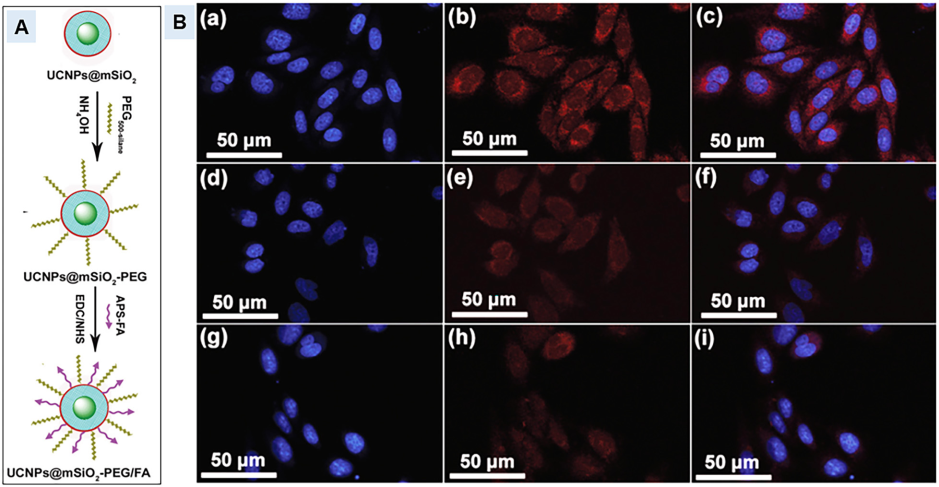
(A) UCNPs@mSiO2-PEG/FA复合纳米球的合成示意图
(B)在37°C下与DOX-UCNPs@mSiO2-PEG/FA(a)–(c)DOX-UCNPs@mSiO2-PEG(d)–(f)和DOX-UCNPs @mSiO2-PEG/FA +游离FA(g)–(i)孵育1小时的HeLa细胞的共聚焦激光扫描显微镜(CLSM)
02
癌症生物标志物检测的纳米传感探针
I. 基于纳米材料的电化学探针
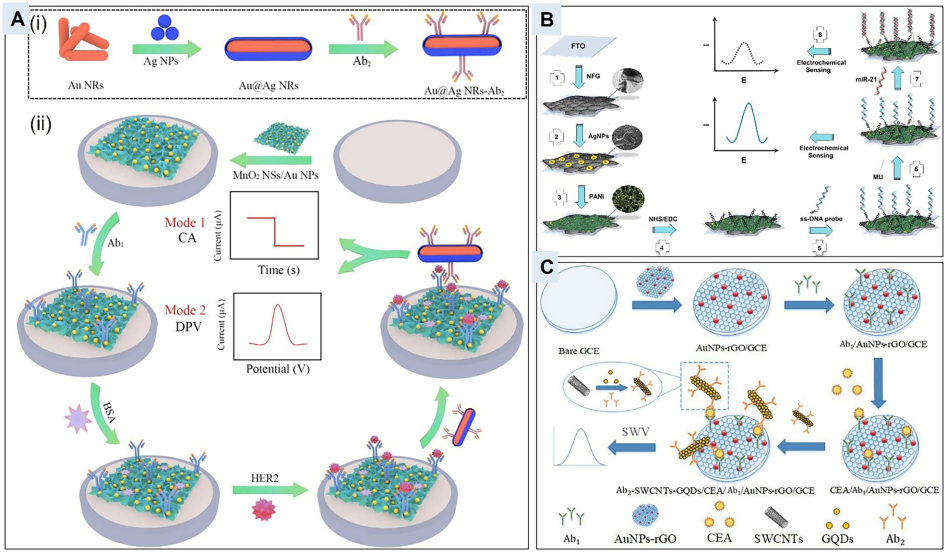
基于纳米材料的电化学探针。
(A)(i) Au/Ag NRs-Ab2 的合成过程和 (ii) 双模电化学免疫传感器的逐步设计和开发示意图
(B) 纳米复合材料的逐步制备示意图
(C) 使用单壁CNTs@GQDs纳米复合材料制备双信号放大非酶电化学传感平台示意图
II. 基于纳米材料的光学探针
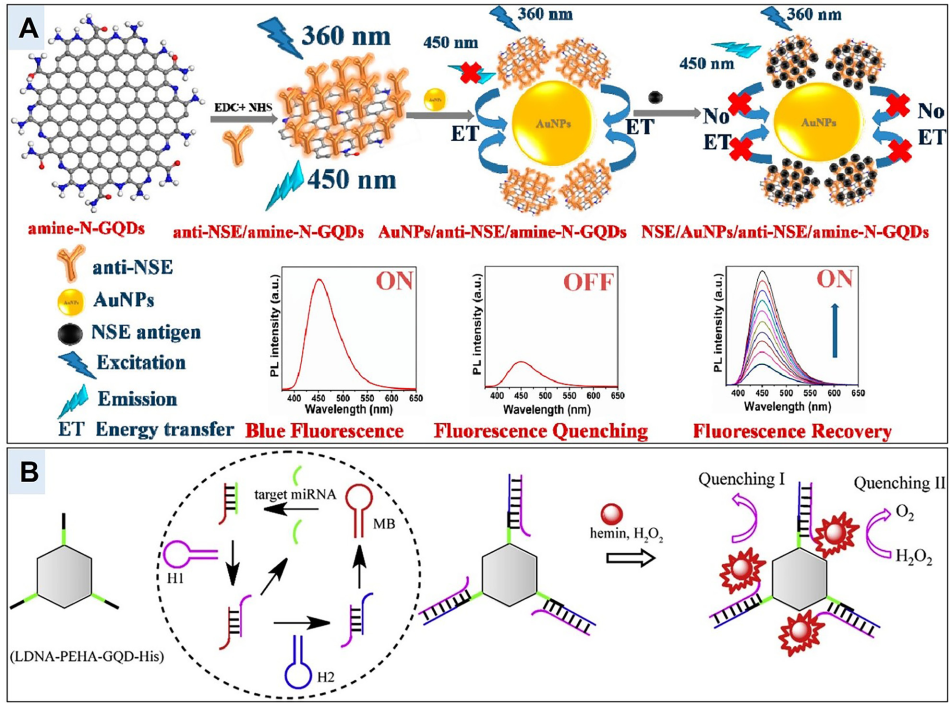
(A)基于胺功能化和氮掺杂的GQDs(胺-N-GQDs)荧光生物传感器用于小细胞肺癌生物标志物检测的机制示意图
(B)通过分子信标双循环扩增策略检测miRNA的PEHA-GQD-His光学探针设计合成过程示意图
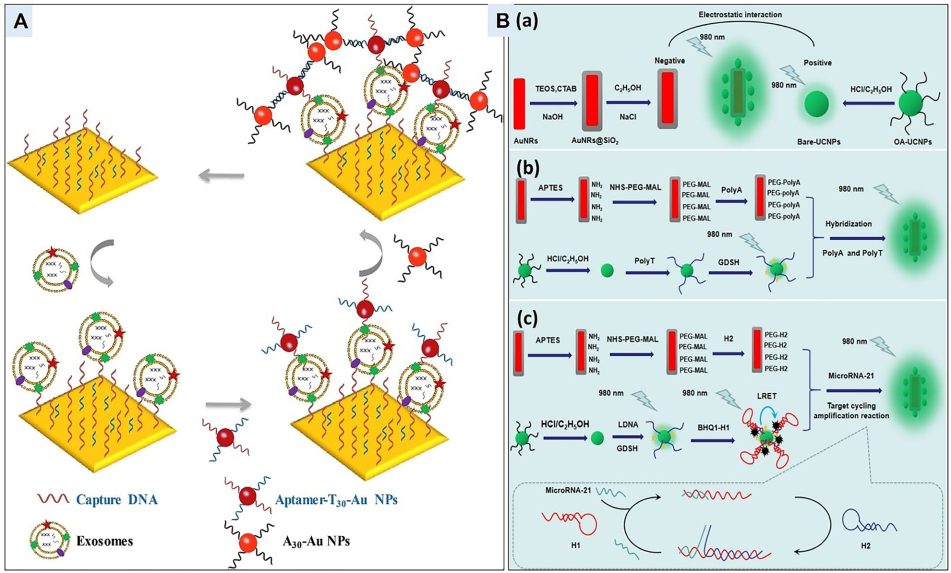
(A)用于开发基于适配体的 SPR 传感器以灵敏检测外泌体的双重 AuNP 辅助信号放大策略示意图
(B)(a)绿色荧光 AuNRs@SiO2-UCNPs 纳米复合材料发光强度的增强和(b)和(c)AuNRs SPR 效应传感平台的设计示意图,用于灵敏检测 miRNA
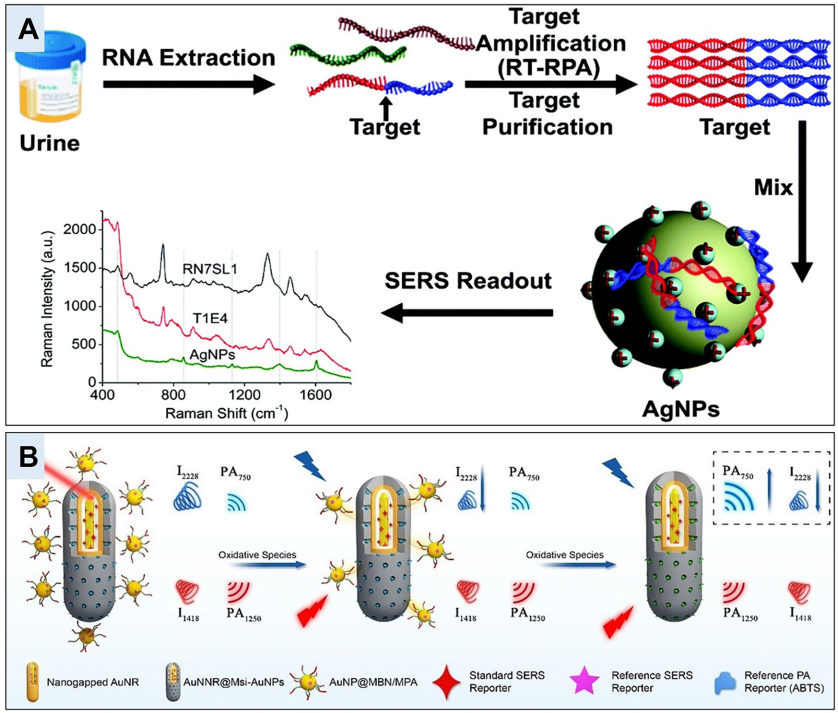
(A) 使用从尿液中提取的总 RNA 和扩增策略直接检测多种 RNA 生物标志物的无标记光学 SERS 传感探针的开发示意图.
(B)产生核-卫星纳米结构的双比率SERS信号的示意图,用于检测炎症和癌症过程中产生的氧化物质。
结论
Conclusions
本综述讨论了几种用于癌症增殖综合早期诊断的工具,并认为生物成像和生物传感是癌细胞追踪的两种主要方法。重点考虑了荧光显微镜这种简化的活细胞成像技术的特征,并简要研究其随时间的逐渐演变。同时解释了负责FM操作的主要光物理机制。考虑使用基于 AIE、PET、FRET 和 UCL 的成像探针,重点关注这些过程的临床实验弊病。
此外,还梳理了使用各种癌症生物标志物作为生物识别元件以及纳米级材料作为电极表面改性剂、催化剂和信号放大器用于电化学和光学生物传感的研究。由于其生物相容性和大面积体积比,不同类型的纳米材料被广泛研究,以修饰工作电极的表面。修改和功能化程序可以增强电极的电子转移能力和传感器的分析性能。尽管纳米级材料在癌症诊断方面的潜力已经得到了多年的证明,但必须解决一些挑战才能促进这些材料的临床转化,例如合成具有可重复的化学、生物、电学和光学特性的纳米级材料;改进的表面改性工艺,以最大限度地减少生物分子的非特异性吸收,并增强生物传感器在复杂样品中的稳定性;开发用于血清、唾液、尿液、血液和肿瘤细胞的新型癌症生物标志物,以支持各种癌症的早期诊断。
参考文献:
Sachin Kadian, Shubhangi Shukla, Roger J. Narayan; Probes for noninvasive biological visualization and biosensing of cancer cells. Appl. Phys. Rev. 1 December 2023; 10 (4): 041304.
原文链接:
https://doi.org/10.1063/5.0166740

编辑 | 刘帅
审核 | 医工学人


本篇文章来源于微信公众号: 医工学人