阅读导言

文章开始前,我们先抛开这一长串的题目,聊一聊我们更加“熟悉”,也大概率曾经在医院里接触过的东西——超声成像。
超声成像或许可以说是人类历史上最伟大的发明之一。它不像是电灯泡、计算机、汽车等发明显而易见的改变了我们的生活。但我们可以说,一个人一生,从尚是母亲子宫中孕育的小生命时,就不可替代的受益于超声成像的发明,专业的医生在超声成像设备的帮助下,对人体内的器官和组织进行观察,将细微的、不显于体表的病患暴露出来,成功挽救了数以亿计的病人。
由于其无创、零辐射、高成像速率等特性,使其与X光、MRI等其余成像方式,在应用场景、应用方式上有着明显的优势和区别。超声成像设备和装置,也随着计算机科学、材料科学、电子科学的发展,不断呈现出新的存在方式。近些年,超声成像设备也逐渐摆脱人们的传统印象——大体积、操作复杂、使用门槛高,走向小型化、智能化。
说到这里,就该本篇文章的主角出场了。本次介绍的工作,就是在这一趋势影响下的最新的研究进展,研究人员成功将体积庞大的超声成像探头,集成在一块小小的粘性贴片上——长宽2cm,厚度为3mm。
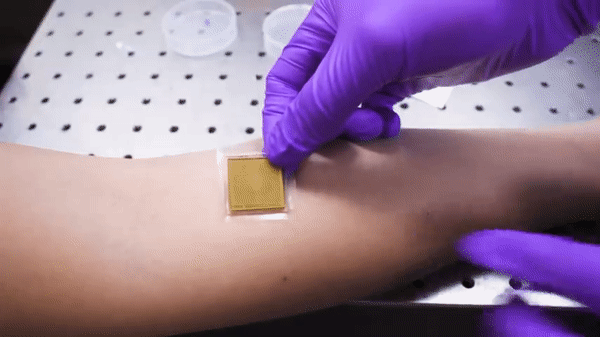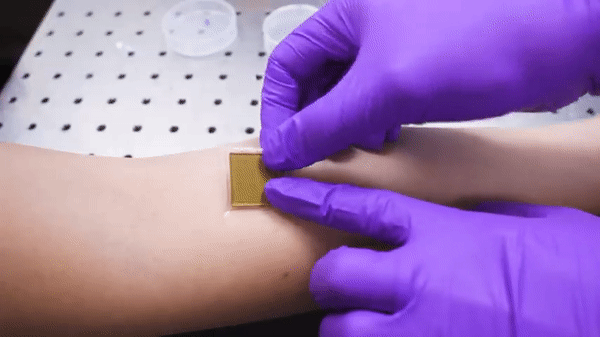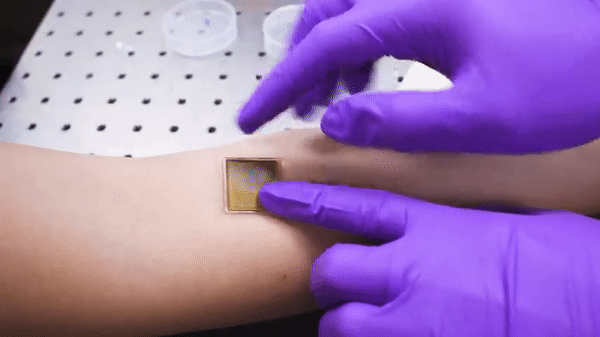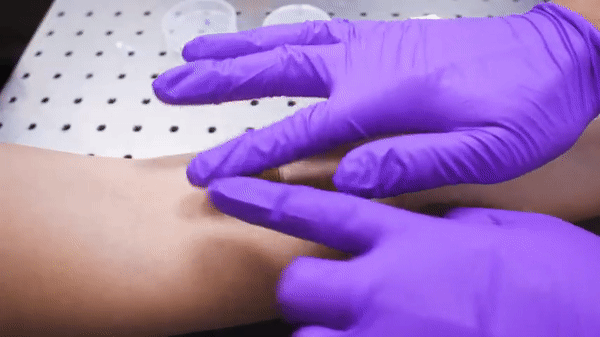
同时这块小小的贴片还可以在长达48h的时间内对人体内器官和组织进行连续的成像,在此过程中,你也不用像是在医院B超检查床上那样躺着一动不动——你可以蹦跳、跑步、骑车,健身,都不会中断成像过程,甚至如果你感兴趣的话——你还可以仔细观察到运动过程中血管和内部器官的运动。
听起来似乎有些神奇。它是如何实现的呢?有哪些有趣的应用呢?这种成像贴片目前又有哪些的限制呢?如果对这些问题感兴趣的话,文章剩余的部分,或许会给你一部分的答案。
写在开始前
本文属医工学人原创论文解读系列。大部分内容材料引自论文原文,每段前后分别有段落“导读“和“总结”,帮助非相关领域的研究者、学生、工程师、医师更好地理解论文的内容。
选段导读:为了解决这个问题,相关领域的研究者和工程师之前都提出了哪些可行的解决方案呢?
选段总结:简单来说,当前的可穿戴超声设备大致分为两种……。
研究摘要
对内部器官进行连续数天的成像可以提供人体健康状况和疾病诊断方面的重要信息,并有助于人们深入了解发育生物学。本研究设计了一种生物粘附超声(BAUS/Bioadhesive ultrasound)装置,该装置由一个薄且坚硬的超声探头,通过一种柔软、坚韧、抗脱水、生物粘附的水凝胶-弹性体混合物制成的粘合剂牢固地粘附在皮肤上。BAUS装置可以对包括血管、肌肉、心脏、胃肠道、膈肌和肺的各种内部器官进行48小时连续成像。BAUS装置可以作为对各种疾病进行诊断和监测的工具。
该研究想要解决的问题是什么?
能够以无创方式连续监测人体生理的可穿戴设备代表了现在精准医学和数字医学的关键趋势。尤其是深层组织的生理学信息,包括内部器官的信号和动力学参数,包含了健康和疾病的重要信息。
尽管目前的可穿戴设备已经成功地记录了来自皮肤的物理和化学信号,例如心电图数据、汗液代谢物和电解质,但各种内部器官的临床级成像仍然是可穿戴设备领域的核心任务和挑战。
零辐射的超声成像允许临床医生评估组织和器官的功能,诊断各种疾病。如果在几天到几个月内对内部器官进行连续超声采样并进行成像,可以帮助临床医生监测健康状况,观察疾病进展,并且评估疾病风险,这也能够促进对发育生物学的更多发现和更深理解。
选段总结:简单来说,我们平日里去医院做的超声检查,能看到的只是人体一瞬间或是一小段连续时间里的内部状态,若是对一些需要长期观察或是动态监测的疾病,传统的超声检查或许就帮不上忙了——除非你和医生能够保持相对静止的姿态,在检查台上躺一整天。这时我们就需要一个连续且不影响我们日常活动的成像方案。
已有哪些解决方案?它们有什么局限?
选段导读:为了解决这个问题,相关领域的研究者和工程师之前都提出了哪些可行的解决方案呢?同时在实现过程和使用过程中又存在哪些问题呢?
可穿戴超声设备具有对内部器官进行连续成像的潜力。传统的可穿戴超声成像通常依赖于在皮肤上安装的庞大的超声探头,这些探头由机器人系统或者机械固定装置,如皮带和胶带来固定,这使得患者不方便移动,并且佩戴时不够便利与舒适。另外,较厚的超声探头和由探头产生的高压使得传统的可穿戴超声成像仅适用于有限的身体部位,如肌肉。例如,将传统的超声探头机械地安装在病人颈部来对颈动脉、颈静脉和迷走神经进行成像可能会导致病人窒息。
虽然可延展的超声成像设备在佩戴性方面得到了改善,但它仍然受到了诸多限制,包括低成像分辨率、身体运动期间不稳定的成像质量、连续成像时间短(1小时),易受装置故障影响。(连续成像持续时间被定义为设备可以附着或佩戴在皮肤上的最长时间。)这些限制主要来源于装置的设计问题,设备由可延展基板上的压电元件组成(图1A)。尽管可延展的基底可以随着皮肤一起变形,但是它限制了元件的密度(每平方厘米156个单元),并且与背衬层和匹配层不相容,导致成像分辨率低。另外,当基底在身体运动下随着皮肤变形时,元件的空间和角度位置发生了不可预测的变化,而这影响了设备的成像稳定性。
此外,现有的可穿戴超声设备,无论是刚性的还是可延展的,都主要依靠水凝胶或弹性体耦合剂将超声传递到皮肤上。然而,水凝胶耦合剂通常会在几个小时后脱水或从皮肤上脱落,并且弹性体耦合剂由于阻尼太大从而不能对深层器官成像。
选段总结:简而言之,当前的可穿戴超声设备大致分为两种,一种是将庞大的超声探头通过机器人系统或者机械固定装置和人体牢固的绑定在一起,这种方案的问题是患者不便移动、舒适度不足、以及可能造成额外的行动负担甚至健康风险。另一种方案是将超声探头制作在可拉伸的柔性基底上,贴附在人体皮肤上一同运动。这种方案的问题是换能器密度受限(相比于刚性探头),粘附性不足,以及随着身体运动造成的换能器位置随机误差。
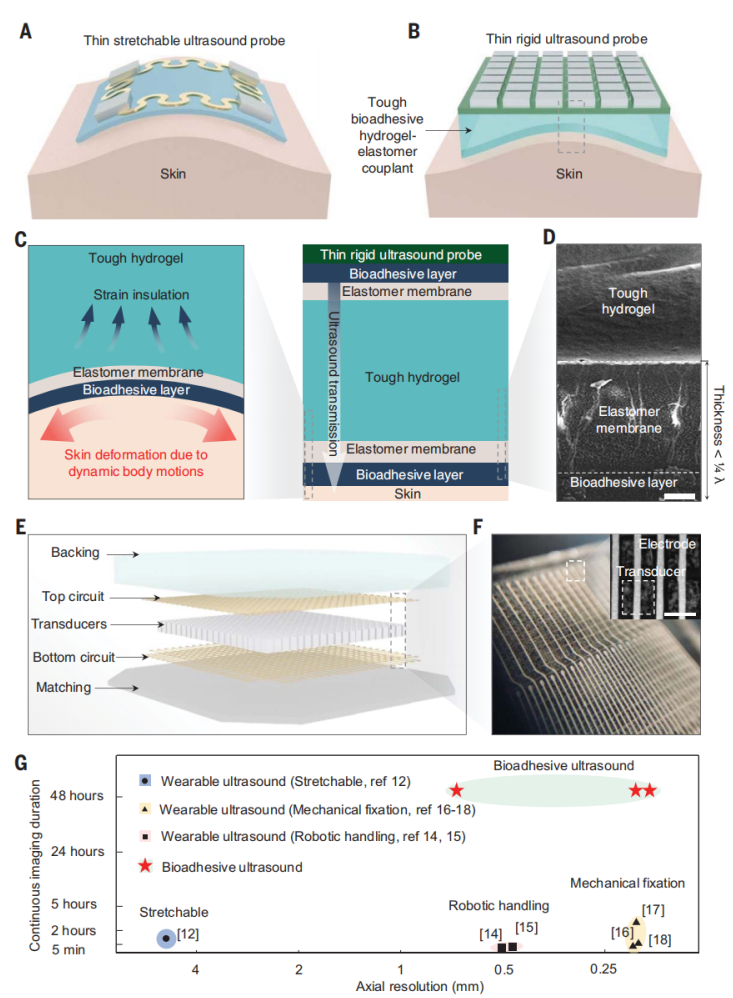
图1.BAUS装置的设计和成像性能
新的解决方案如何克服上述问题?
选段导读:介绍了以上其他解决方案的缺点,那么本次介绍的研究提出的BAUS装置能否克服以上这些问题呢?如果可以,又是采取了怎样的方案呢?
本文报告了一种生物粘附超声(BAUS)装置,该装置由一个薄且坚硬的超声探头组成,并通过一种柔软、坚韧、抗脱水材料制成的耦合剂层和生物粘附性水凝胶-弹性体混合物牢固地粘附在皮肤上(图1,B到D)。
BAUS探头有着高密度的元件(每平方厘米400个单元),这使得它在身体动态运动下具有稳定的元件位置,以及在长期应用中有着较高的可靠性。BAUS耦合剂能有效地传递声波,使BAUS探头免受皮肤变形的影响,并在48小时内保持牢固舒适的皮肤粘附力。
BAUS探头由中心频率为3、7或10MHz的高性能压电元件阵列组成(图1,E和F)。每个元件由BAUS探头的顶部和底部电路控制。这些电路可以通过三种技术制作:3D打印(图1F)、激光刻蚀和光刻,他们分别能达到100、10和1μm的电路线分辨率。同时,利用优化后的声学匹配层覆盖在底部线路上从而增强到皮肤的声波传递能力,将优化后的声学背衬层覆盖在顶部电路上来抑制共振效应。BAUS探头由一层环氧树脂密封,使其在长期应用中具有高稳定性和可靠性。本文还设计了一种即插即用的输入输出,并将其与柔性扁平电缆连接。BAUS探头的厚度为3mm,长度和宽度为1-2cm,重10-40g。
BAUS耦合剂由柔软而坚韧的水凝胶组成,该水凝胶由壳聚糖-聚丙烯酰胺互穿聚合物网络(10%重量)和水(90%重量)组成(关于BAUS耦合剂的制造细节,参见论文附件材料和方法)。水凝胶用聚氯乙烯制成的薄弹性体膜(厚度小于40μm)封装以防止水凝胶脱水,同时,耦合剂的表面保持干燥能提供舒适的皮肤接触性。聚氨酯膜是用聚丙烯酸与N-羟基琥珀酰亚胺酯(NHS酯)结合制成的,并与水凝胶形成牢固的结合。水凝胶-弹性体混合物进一步用一层薄的生物粘附层(厚度小于10μm)覆盖,生物层则通过共聚聚(乙二醇)二丙烯酸酯、丙烯酸2-乙基己酯、丙烯酸和丙烯酸-NHS酯合成。生物粘合剂中的羧酸、乙基和己基可以形成物理键,例如氢键和与皮肤的静电相互作用;生物粘合剂中的NHS酯基团可以与皮肤形成共价酰胺键。弹性体膜和生物粘附层的总厚度小于声波波长的四分之一,这可以最小化BAUS耦合剂的声衰减(图2D)。
选段总结:本文的研究者用相当巧妙的方式设计出了一种BAUS装置,利用刚性换能器阵列+抗脱水耦合剂组合的方式,一方面克服了直接将传统的超声探头机械绑定在人体上带来的不便,另一方面也克服了直接将换能器集成在柔性基底上带来的密度受限的问题。同时也在一定程度上结合了这两种方式各自的优点:成像稳定清晰以及方便佩戴。(形象一点的说,采用了“刚柔并济”的方案)
对BAUS装置关键指标的测试方法及结果
选段导读:设计出的BAUS装置的一些关键指标数据如何?如何测定?为什么这些指标对该应用非常重要?
为了定量地验证BAUS装置在动态身体运动的情况下能够牢固地附着在皮肤上,本文开发了一种刚性体装置模型,通过柔软的耦合剂层附着在皮肤上(图2A)。
当皮肤被施加应变拉伸时,耦合-皮肤界面边缘会产生裂纹并扩展。裂纹扩展由能量释放率G(单位面积内,裂纹扩展时耦合皮肤系统中释放的弹性势能)驱动,由界面韧性Г(裂纹单位面积扩展所需的能量)抵抗。在图2B中,我们计算耦合皮肤系统在平面应变条件下的能量释放率G,器件长度L为2cm,皮肤的典型应变为20%。为简化计算,皮肤和耦合层均为杨氏模量均为100 kPa的不可压缩线性弹性材料。当能量释放速率高于界面韧性,即G >Г时(图2B中未遮挡区域),裂纹在界面上扩展,器件脱离皮肤。当刚性器件在没有耦合剂(耦合剂厚度H = 0)的情况下附着在皮肤上时,其韧性约为1J/m2,刚性器件会从皮肤上脱落。相比之下,当刚性器件通过BAUS耦合剂粘接在皮肤上时,无论是在空气中还是在水下,其界面韧性都超过500 J/m2(图2C),此时无论偶联剂厚度如何,器件都能牢固地粘接在皮肤上。
为了评价BAUS耦合剂在猪皮上的粘附性能,我们进行了标准的90°剥离试验(ASTM D2861),以测量弹性体膜通过生物粘附层粘附在猪皮上的界面韧性(有关测试的细节,请参阅材料和方法)。由于猪皮与人的皮肤相似,我们选择猪皮作为评估粘附性能的模型组织。弹性体膜可牢固地粘附在猪皮上,界面韧性为853J/m2。当粘附样放置于空气中(相对湿度30~50%;24°C),48 h后界面韧性降至756J/m2;当试样置于水中模拟潮湿环境时,48小时后界面韧性降至518 J/m2。这些结果(图2,C和E)表明,在干燥和潮湿的环境中,生物黏附层能够将BAUS装置牢固地粘附在皮肤上超过48小时。通过BAUS偶联剂的一端进行剥离,可以将BAUS器件与皮肤分离的同时不留下任何残留(见图S12)。相比之下,典型液体和固体水凝胶耦合剂和弹性体耦合剂(包括硅胶、聚氨酯和水烯)界面韧性都小于10 J/m2,从而超声探头不能在皮肤上稳定粘附。虽然3M VHB丙烯酸胶带在空气中48小时以上仍能保持较高的界面韧性(大于456J/m2),但是在水中界面韧性下降至27 J/m2,在潮湿环境中将可能导致粘接失败。

除此之外,研究团队还分别对BAUS装置的佩戴舒适度、耦合剂的声学性能、探头信号性能、成像分辨率、稳定性、热学性能分别进行了定量实验。限于篇幅原因不详细展开,感兴趣的读者可以自行阅读原文。
选段总结:能量释放率G与界面韧性Г的相对大小关系决定了BAUS装置能否牢靠的黏附在皮肤上。前者(能量释放率G)驱动裂纹扩展,后者(界面韧性Г)抵抗裂纹扩展,BAUS装置的界面韧性Г会随着时间、环境温湿度的变换而变化,当G>Г时装置会逐渐脱落。最终经实验测定,在48h间隔,空气相对湿度30~50%,24°C的情况下,BAUS始终保持高的界面韧性Г(高于3M VHB丙烯酸胶带),除此之外,研究人员还详细测定了BAUS装置的声学性能、探头信号性能、成像分辨率、稳定性、热学性能。
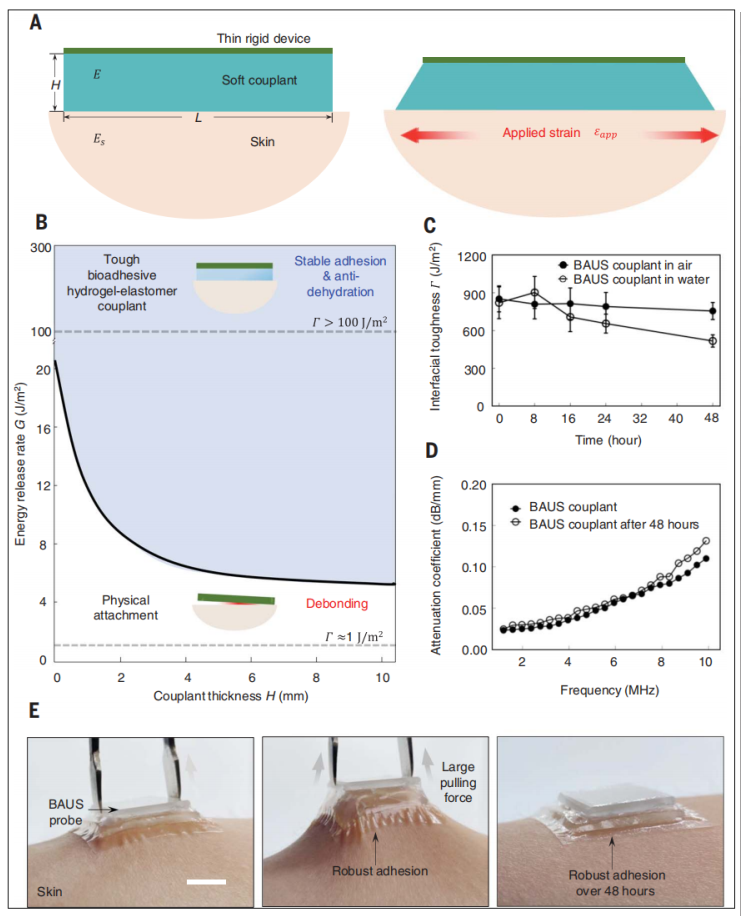
图2. BAUS器件的附着力和声学性能
该研究未来可以进一步应用于哪些领域?
选段导读:这种超声贴片未来可以适用于哪些场景?可能解决哪些问题?
1.心脏疾病诊断:BAUS设备可以在动态身体运动(例如角度高达 ±30°的颈部旋转)下提供颈静脉和颈动脉的48小时连续成像(图3B)。这是BAUS设备在颈部的强大粘附力、BAUS探头的高成像分辨率以及 BAUS 探头孔径(2 cm x 1 cm)提供的大声学窗口等因素的共同作用结果。BAUS 成像结果显示,受试者的颈静脉直径从坐姿或站姿到仰卧位依次增加(图3C)。颈静脉直径的变化与右心房压力密切相关,因此可用于诊断心脏疾病,如心力衰竭和肺动脉高压。
2.血压监测:BAUS 成像结果进一步提供了颈动脉48小时连续血流速率和血压波形数据(图3,D至F)。例如,我们观察到受试者在0.5小时体育锻炼前后的血流率(从65到117 cm/s;图3D)和收缩压(从115到168mmHg;图3E)(数据采集和血压计算的详细信息见材料和方法)。此外,从0.5小时慢跑后测量的血压波形(图3E右图),我们可以看到每个心脏周期的收缩压峰值下降比运动前更陡,可能是由于运动引起的颈动脉血管舒张。
3.肺部疾病(例如COVID-19)监测:图4,A和B,以及图S33展示了粘附在受试者右胸(纵向)上的 3-MHz BAUS 相控阵设备获得的肺部成像结果(图4A)。BAUS系统可以提供48小时对肺部关键特征的连续成像,包括胸膜线和A线。BAUS 设备还能够连续稳定地对慢跑和骑自行车等身体运动下的肺进行成像。BAUS 成像显示受试者在48小时内有一条平滑的胸膜线和重复的A线,表明肺部健康、正常通气。尽管肺超声检查已被证明是诊断COVID-19患者的有效工具 ,但它主要在医院用于不频繁和不连续的肺部成像。相比之下,可穿戴BAUS系统可以在家中持续监测可能感染的COVID-19患者的症状。
4.运动状态监测:图4,C和D,展示了3-MHz BAUS相控阵设备在0.5小时体育锻炼前后粘附在受试者右前肋下区域获得的膈肌运动的成像结果。BAUS成像显示,相较于训练前的安静呼吸,训练后的横膈膜运动在幅度和频率上更加剧烈。
图4E 展示了附着在受试者左胸的3-MHz BAUS相控阵设备获得的心脏成像结果(通过心尖四腔视图可视化)。BAUS系统可以提供四个心腔动态的48小时连续成像:右心室、右心房、左心室和左心房。BAUS设备还能够连续稳定地对慢跑和骑自行车等身体运动下的心脏进行成像。例如,我们观察到在0.5小时的体育锻炼后,左心室的大小会显著增大。心脏腔室的连续图像可以进一步处理,以计算心脏应变的动态参数,这是指示心肌病的重要参数。
5.饮食监测:图4F展示了胃部成像结果,通过粘附在受试者上腹部皮肤上的3-MHz BAUS相控阵设备获得。BAUS成像系统提供胃窦横截面的48小时连续成像。例如,一旦受试者喝了450毫升果汁,我们观察到胃窦延长(图4F)。在接下来的2小时内,由于胃排空,胃窦横截面积逐渐减小(图4F)。
选段总结:研究者利用BAUS装置对一些常见的人体组织和器官进行了长时间内部成像,获得了较好的时空分辨率,也尝试了一些实用而有趣的应用场景。由于其可以长时间准确的监测人体关键的器官和组织形态,并分析出相应的生理参数,为健康监测和疾病诊断提供牢靠而准确的数据。例如:心脏病、血压、肺部疾病(COVID-19)、运动健康、食量监测等。
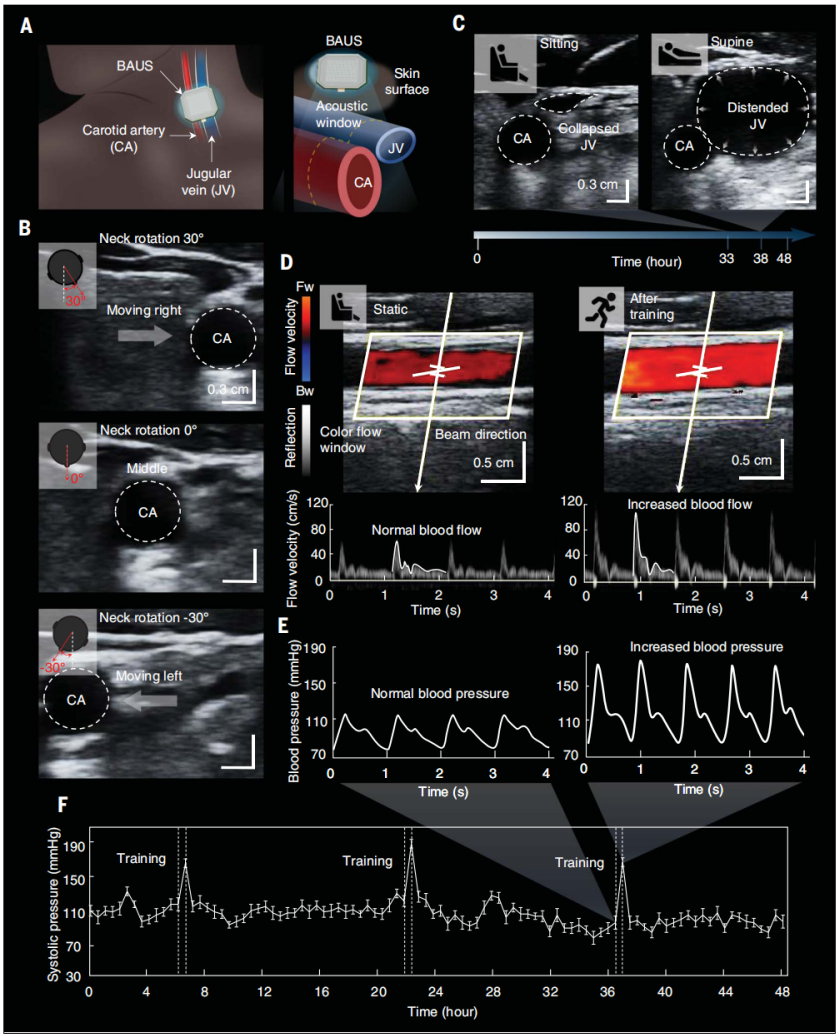
图3.血管长期连续BAUS成像
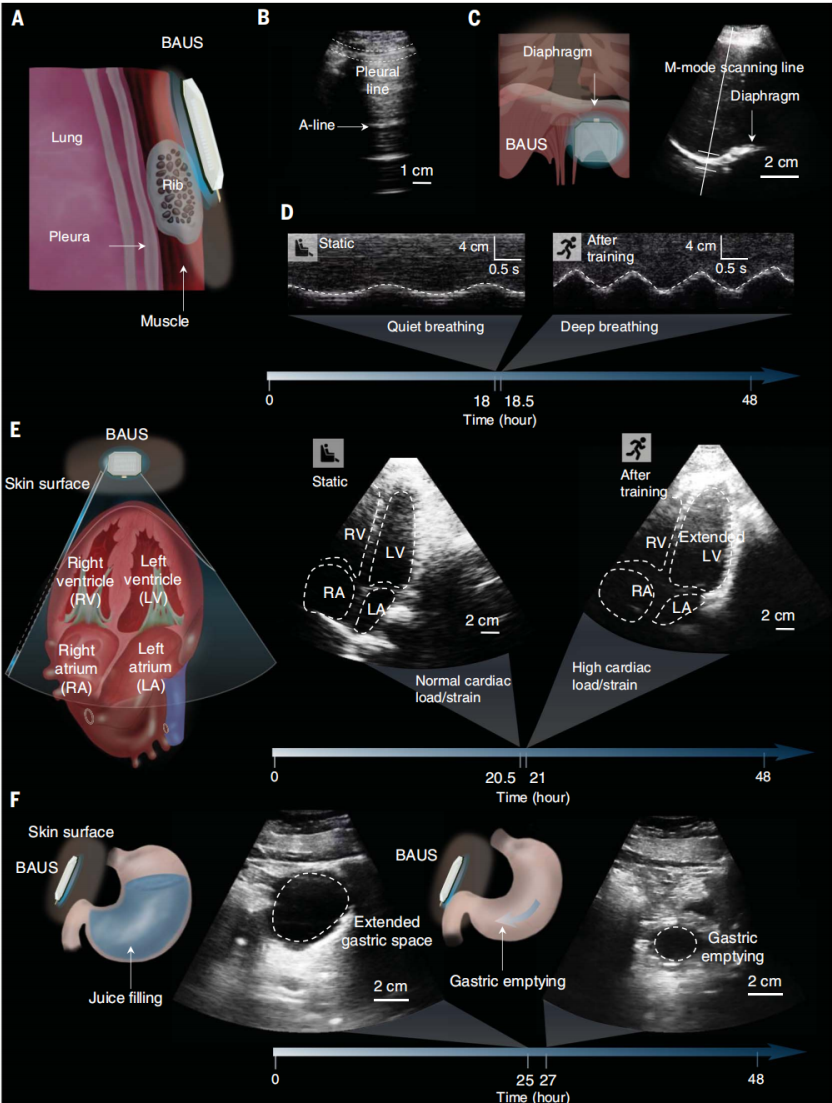
图4:肺、隔膜、心脏和胃的长期连续BAUS成像
未来的工作
选段导读:文章的最后,研究人员还提出了目前工作尚存在的一些问题,以及未来的工作方向。
尽管 BAUS 探头的成像分辨率优于现有的可穿戴超声设备(图1G),未来可以进一步改进BAUS探头以获得更好的成像质量。
当前 BAUS 探头的间距相对较大(0.5 毫米),并且会产生栅瓣,尤其是在7MHz和10 MHz的BAUS 探头中。虽然通过使用平面波复合方法可以减轻栅瓣伪影,但将来 BAUS 探头的间距可以进一步减小来消除伪影。虽然目前的 BAUS 探头没有仰角聚焦,但可以将薄型 (<1 mm) 仰角透镜添加到将来的 BAUS 探头中用于仰角聚焦以获得更好的成像质量,尤其是对于深部器官的成像。
由于目前的工作重点是设计和制造BAUS设备,我们使用外部系统(Verasonics Vantage系统)进行数据采集。尽管数据采集系统的规模很大,但BAUS设备可能会很快应用于临床环境中的非移动成像中,例如对重症监护病房患者的长期成像。此外,由于床旁超声设备(例如 GE VScan、Butterfly IQ 和 Phillips Lumify)的数据采集系统已经小型化到手机大小,因此 BAUS 的数据采集系统可以在未来做的更小。除了临床应用之外,BAUS 成像平台还可以以无创方式提供组织和器官(包括胚胎、肿瘤和大脑)发育的长期连续成像 。
选段总结:
研究人员提到了当前工作尚存的两点问题。第一点是BAUS探头形状和位置设计上的不足,造成成像质量上的缺失。
第二点提到了,同时也是那些不太了解超声设备工作方式的读者,最容易产生误解的地方:即完整的超声成像设备是由探头+后端系统组成,本文提出的BAUS装置只是集成了超声的探头端,而后端系统才是整个成像设备体积最大的部分,目前最小的后端系统也只能做到和智能手机体积大小相仿。因此本文的BAUS装置还是得通过较长的线束连接到外部成像系统上进行成像,尚不能随时随地的移动成像。不过,研究人员也表示,实验室未来工作的方向是将BAUS与后端系统进行小型化集成,并利用智能手机和AI算法进行随时随地、方便快捷的健康诊断和监测。
或许未来有一天,我们只需要坐在家里,撕开包装轻轻一贴,打开智能手机,就能获得和医院相同质量的超声图像,并借助AI算法即时得到疾病诊断与健康建议。
论文链接:https://www.science.org/doi/10.1126/science.abo2542
感谢您的耐心阅读到这里,论文解读系列是医工学人长期展开的、同时面对本领域研究者与科普读者的系列活动。
若本系列对您了解相关研究领域最新进展有所帮助,欢迎您关注医工学人公众号,第一时间获取最新的更新内容。
也欢迎各位读者的转发、点赞与收藏,好的idea值得分享。
Plus:若您对本文相关内容仍有疑惑,也欢迎后台联系我们,我们可以帮助您联系文章的作者,促进更近一步的交流。
本文系医工学人原创内容
诚邀您的来稿
媒体转载联系授权可添加下方微信

医工学人简介
医工学人是在医疗科技创新与医工交叉背景下成立的多高校学生学术组织。旨在建立医学、工程学领域研究者的对话渠道,创造交流分享医工交叉前沿技术的优质平台,推动医疗科技创新与医工交叉融合。
目前组织内共有两百多位来自复旦大学、西安交通大学、上海交通大学、清华大学、浙江大学、中国科学技术大学、各高校附属医院等30余所重点高校、医院及科研单位医工学科相关的医生、学生、专家学者等。欢迎志同道合的你加入我们!
医工学人报名请添加社群发起人微信(备注姓名+单位),请简单介绍一下想加入医工学人交流群的原因和感兴趣的方向,方便我们管理社群,谢谢!


本篇文章来源于微信公众号: 医工学人